トップニュース 「第33回 製薬協政策セミナー」を開催 日本発の革新的な新薬創出に向けて ~絶え間ないイノベーションを生み出すヘルスケアエコシステムの構築~
新型コロナウイルス感染症(COVID-19)の拡大は、国として新薬の創出力を高める必要性とその基礎となるイノベーション環境の構築等、日本の製薬業界にも大きな課題を投げかけました。2022年3月14日にライブ配信形式で開催された「第33回 製薬協政策セミナー」では、創薬エコシステムや、ライフサイエンスクラスターの整備、ベンチャーやスタートアップの育成、産学官連携強化、グローバルマインドセット等、日本が世界的新薬創出国であり続けるために必要なテーマが議論されました。以下はセミナー内容の採録です。
日本発の新薬が花開く未来へ 産学官によるヘルスケアエコシステム加速を
第1部 ヘルスケアエコシステムを構築・発展させるには何が必要か?
■特別講演
製薬大国復活へ 経済安全保障整備
衆議院議員 自由民主党 経済安全保障対策本部 座長 甘利 明 氏
国家の安全を維持し、国民の命と財産を守る──。安全保障といえば、多くは軍事や外交上の問題と捉えられがちだが、近年、これが経済分野へと拡大している。例えば、広大な市場を有する国が、貿易を通じて相手国を自国に依存させ、その上で内政を干渉、政策誘導を行うなどの例だ。
一方、旧来型の安全保障も様相を変えている。サイバー攻撃やSNS(交流サイト)などによる世論の誘導、さらには相手国へ自国文化を浸透させ戦意の喪失を促すなど、脅威はさまざまである。

こうした状況に鑑み、日本政府は「経済安全保障推進法」の制定を最重要課題とし、今通常国会での成立を目指す。同法案は4つの柱からなる。
第1は「サプライチェーン(供給網)の強化」だ。今回の新型コロナウイルス感染症との戦いで、真っ先に指摘されたのは、マスクや医療用ガウン、医療用手袋などの供給体制の脆弱(ぜいじゃく)さだった。安全保障に関わる重要物資には、供給途絶が国民の生命に影響する医薬品をはじめ、半導体や希土類金属などがある。同法案では、これらを国が選定し、サプライチェーンの脆弱性を洗い出し、さらに克服する仕組みの確立を目指す。
第2は「基幹インフラの安全性確保」である。通信、金融といった6分野14業種の基幹インフラについて国が審査。安全保障に関わる問題の有無を洗い出す。例えば、使用されるデジタル機器などの発注先が信頼できる企業か否か。マルウェアが仕組まれていないかなどを精査する。
第3は「重要技術の研究開発推進」だ。第1、第2の柱とは裏腹に、日本が技術を通じて、世界になくてはならない存在となり、これを経済安全保障上の抑止力とする。研究開発の促進には、重要技術の選定が不可欠だ。そのためのシンクタンクとして政策研究大学院大学に、自然科学系の研究科を新設する構想もある。
創薬は日本が有する重要技術だ。世界で創薬が可能な国は、米国、欧州の一部、日本の3極だけである。ところが、新型コロナウイルス感染症のワクチン開発では遅れをとった。国内にワクチン開発、生産能力を持つことは、国民の健康保持はもちろん、経済安全保障という観点からも極めて重要だ。一方でワクチンは常時生産するものではない。平時はバイオ系医薬品の製造ラインとして使い、有事はワクチン製造ラインに切り替えるなどのなどの仕組みも構築すべきだ。国産ワクチン、治療薬を望む国民の声をよく聞く。日本のものが一番信用できるという証左だ。日本が名実ともに創薬大国であるよう、官民一体で環境整備をしていきたい。
第4は「特許非公開制度」の導入だ。軍民融合が進む現在、科学技術を民生と軍用に区別するのは難しい。一方、現行の特許制度は公開が原則だ。公開された日本の先端技術が他国によって軍事転用され、日本の脅威となる可能性がある。そこで、国が安全保障上重要と判断した技術を、非公開とするのが特許非公開制度だ。ただし、同制度が民間の研究開発、イノベーション力への過度な制約を生まないよう、適用は最小限にとどめたい。
実はこれら4本柱は、多くの国がすでに備えるものだ。我が国の取り組みが他国と一線を画するのは、経済安全保障の概念を改めて定義し、法律として体系化したところにある。
課題も残る。セキュリティークライアンス(SC)制度の不備はその代表だ。SC制度とは、機密の漏洩を防止するため、情報へのアクセス権を持つ人物を国が認定するものである。14年に施行された特定秘密保護法では、公務員に関してSC制度に近い仕組みを作り上げた。これを民間へと広げていく考え方となる。国家・国民の安全のため、皆様のご理解とご協力を得られるよう、これからも訴えていきたい。
 講演の様子
講演の様子
■講演(1)
スタートアップ育成 多角的に支援
GRiT Partners法律事務所 所長弁護士/内閣府バイオ戦略有識者 吉澤 尚 氏
創薬を取り巻く環境が大きく変わっている。低分子医薬品の開発が中心だった20世紀は、アカデミアと製薬会社の役割分担が明確であり、研究開発も基礎から応用、そして産業実装へと進む、単純なものだった。ところが、バイオ医薬品や再生医療、遺伝子治療など、多様なモダリティーが登場した今日、創薬には多分野の機関や専門家が複雑に連携する仕組みが必要になっている。

例えば、バイオ医薬品の開発では、アカデミアと製薬企業の他、バイオベンチャー、ベンチャーキャピタル(VC)、医薬品開発業務受託機関(CRO)、医薬品製造受託機関(CMO、開発製造受託機関(CDMO)などが関わる。CROとは製薬企業の依頼によって臨床試験などを請け負う機関だが、開発段階ごとに必要なスキルが異なり、連携はますます複雑化している。また、個別化医療を見据えた創薬には膨大なデータの利活用が不可欠だが、その取得・生成、保管・管理の研究基盤構築にも、多くの専門家の力が欠かせない。
こうした課題を踏まえ、準備しているのが、創薬分野のスタートアップ企業を支援する「ライフサイエンスインキュベーション協議会」である。そのミッションは「国際市場で戦えるライフサイエンス事業を生み出すプラットフォームをつくる」こと。そして「包括的な支援の輪を構築し、2030年までに時価総額累計1兆円のライフサイエンス事業を創出」することだ(図1)。
図1 バイオ戦略のバイオコミュニティの実装と様々なプレイヤーの連携
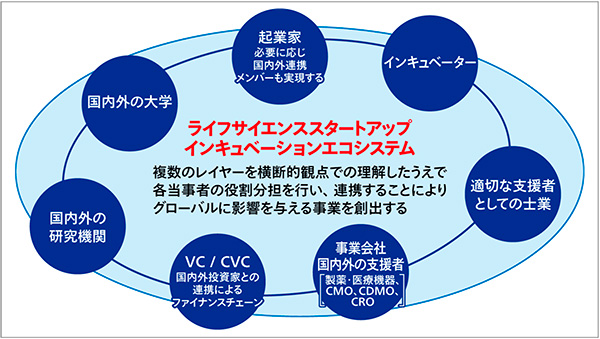
具体的機能は大きく6つ。第1が「複数レイヤーの連携・交流の実現」である。国内外の研究機関や大学、起業家、インキュベーター、士業、製薬会社やCMO、CDMO、CROといった企業、VC、コーポレートベンチャーキャピタル(CVC)などを、適切に連携させる。第2が「政策提言の実施」だ。政府への提言によって、製薬産業の発展を促す。第3は「産業発展に資する情報発信」であり、製薬企業の動きや各論文を伝達、共有する場をつくる。
第4が「事業化に向けた段階的な支援体制の構築」である。創薬実現に向け、本当に機能するコミュニティーづくりを目指す。第5が「ニーズ、シーズ開示の場」だ。創薬ビジネスは特許取得が前提だ。しかし、技術が公知情報になると、特許申請はできない。そこでシーズとニーズのマッチングを行う非公開な場を設け、事業創出を加速させる。第6の「国際機関、他国のクラスターとの連携」では、欧米諸国のクラスターとの連携によるグローバル市場への参入障壁を下げることと、国内の支援体制の向上の2点を目的とする。
同協議会には現在、国内外の多くの大学や研究機関、VC、法律事務所、弁理士事務所などが参画を表明している。活動を通じて日本に、世界に誇れるライフサイエンスのインフラを構築したい。
■講演(2)
グローバルな創薬エコシステム構築
Catalys Pacific, Founder & Managing Partner BT Slingsby 氏
私は米国の医師であり、日本をはじめ、世界中の患者さんに必要な新薬を届けることを目的に、ライフサイエンス分野に特化した独立系VC「キャタリスパシフィック」を創設し、運営を行なっている。
現在、日本の創薬エコシステムは、東京、藤沢、川崎、神戸の4拠点を中心に形成されている。共通するのは、基礎研究から臨床試験、医薬品製造まで「全てを国内で完結させよう」とするマインドセット(思考様式)だ。対して欧米では、各国のバイオ拠点内にとどまらず、グローバルなエコシステムを基盤とする。

例えば、世界的に有名なバイオ拠点である米国ボストンでは、創薬のシーズや技術をハーバード大学などのアカデミアに求める一方、起業家や研究者を世界中から募り、研究・開発の実施や資金調達もグローバル規模で行われる。
創薬エコシステムのグローバル化は、企業と投資家、そして医師と患者さんにも恩恵をもたらす。国際共同治験を実施し開発された医薬品なら、各国への市場参入も容易だ。一国の市場だけでなく、多国の市場を一気に狙えるなら、売り上げ規模は当然拡大する。また、開発品質の向上、研究・開発・製造コストの適正化、更には資金を世界規模で集められる面でも、グローバルな創薬エコシステムにはメリットがある(図2)。
図2 グローバルなマインドセットとは?
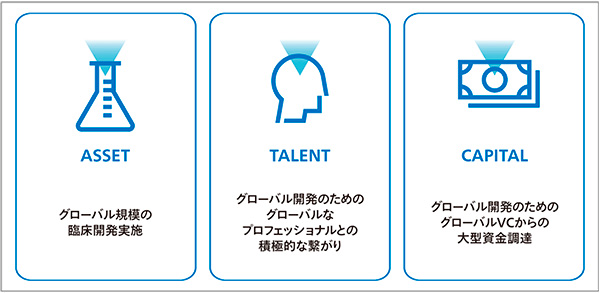
グローバルなエコシステムを基盤とする米国のバイオテック企業は大きな成果を上げている。ここ10年、米国で承認された新薬の半数以上がこうしたバイオテック企業が開発を進めた化合物だ。米国ヘルスケアVCの資金調達額もこの10年で8倍近くに伸びた。これらに鑑み、日本も創薬エコシステムの概念を再定義する必要に迫られている。従来のローカルなエコシステムを脱し、既存のグローバルエコシステムを活用することで、日本のイノベーションをより一層加速させられるのではないか。
キャタリスパシフィックは、日本の創薬シーズや技術を用いて米国でバイオテックを設立・投資を行うアウトバウンド戦略と、米国の創薬シーズや技術を用いて日本でバイオテックを設立・投資を行うインバウンド戦略を実行している。いずれの戦略においても、資金調達はグローバル規模で行なっている。このようにグローバルな創薬エコシステムを活用することで、日本をはじめ、世界中の患者さんに必要な新薬をより早く届けることができると思う。
■講演(3)
社会的インパクトと利益 同時に追求
連続起業家/フェニクシー取締役・共同創業者 久能 祐子 氏
イノベーション(革新・新機軸)とインベンション(発明・発見)──。よく混同される概念だ。一言で表すなら「社会が変わったとき、インベンションはイノベーションになる」となろうか。
両者は誕生の環境も異なる。インベンションは「リスクテイカー型エコシステム」から生まれる。これは「個人の自由度が大きい」「責任と権限が明確」といった要素を持つエコシステムだ。元来、インベンションは多人数ではなく、個人の領分である。新たな次元へと一人で〝跳べる〟環境が重要だ。実際、一人なら跳べるが、大勢が集まり、多くを勉強してしまうと跳べなくなる。そのような経験を多くしてきた。

一方、イノベーションは「リスクシェアリング型エコシステム」から生まれる。こちらは多人数で試行錯誤する環境だ。その実現には「参加者それぞれが自分で決断している」「全員が目標を理解し、なぜそこが目標なのかを理解している」といった要素が大切だ(図3)。
図3 ヘルスケアの将来(4次元的考察が大事)
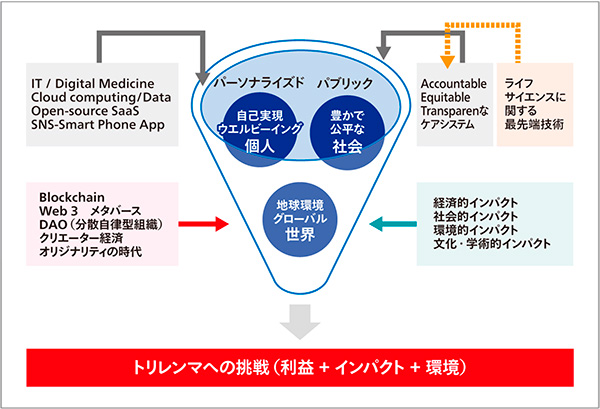
米国・ワシントンDCで創業したソーシャルインキュベーター「ハルシオンインキュベーター」では、こうした考え方を取り入れ、一人での思考の場の確保や、非日常空間での居住、自己効力感の喚起などを念頭に環境を整えた。2019年、この日本版ともいえる「フェニクシー/toberu」を京都で始動させた。日本の場合、多くの優秀な人材が大企業に埋もれている。そこでフェニクシーは企業人が参加できるようにした。
私の周辺の起業家たちが目指すのは、もっぱらプロフィット&インパクト型のビジネスだ。利益とともに、社会課題へのインパクト創出を追求する。従来のように、生み出した利益で社会課題に取り組むのではなく、提供するサービスや商品そのものが社会課題の解決につながるビジネスだ。
16年には、米国で女性による女性のためのファンド「ウィ・キャピタル」を立ち上げた。シリコンバレーのVCによる投資のうち、女性が創設した企業に渡った資金はわずか5%だという事実が、同VC立ち上げの動機だ。現在、ここから企業価値が10億ドル以上の、いわゆるユニコーン企業を3社、輩出している。
創薬も、創薬それだけを考える時代ではない。創薬の営みが、同時に「個人」の自己実現や幸福、「社会」の豊かさや公平さ、「世界」における地球環境やその持続性を実現するものでなくてはならない。これからの製薬企業に求められるのは、これらの取り組みで「利益」と「社会課題解決」と「地球環境保全」を同時に成立させることだと思う。
第2部 ライフサイエンスクラスター形式のキーポイントは何か
■セッション
オープン・公正・合理的な「場」提供
モダリス 代表取締役社長 兼 CEO 森田 晴彦 氏
我々は遺伝子制御技術を使い遺伝子疾患用医薬品をつくっている。例えば遺伝子の量が多すぎて起こる疾患に対しては、そのスイッチをオフにし、逆に遺伝子が足りなくて起こる病気に対しては、その遺伝子をオンにする機能を持つ革新的な治療薬だ。
では東京に本社を置く我々がなぜ研究拠点を米国・ボストンに置くのか。まずは当地がライフサイエンス分野の拠点として、いわゆるヒト・モノ・カネが豊かであることが挙げられる。ハーバードやMIT出身者はもちろん、世界中から集まる優秀な人材、米国でも有数の規模のラボの集積、助成金やベンチャーキャピタル(VC)の投資の大きさなどリソースのすべてが申し分ない水準でそろっている。

さらにボストンには「場」としての魅力がある。英語という共通言語を通じ、上下関係に捉われず誰とでも公平に議論を戦わせることができる。国籍・人種・性別・宗教に関係なく活躍の機会がオープンであり、プロジェクトにおいてゴールポストが動くようなことがない明確さや合理性を持つ環境は、人々が安心して集まることができる要素だ。
加えて「大義や面白さ」というものを心ゆくまで追求できる点が大きな魅力となっている。サイエンティストは、自分の信じるものをとことん突き詰め、トップを目指すことを求める生き物だ。論文や特許などにおいて二番煎じに意味を感じず、圧倒的に世界で一番面白いことをやりたいと思っている。クレージーでとてもできそうにない、でもワクワクすることに挑戦したい人はボストンのそうした空気に引かれて集まってくる。ゲノム編集やmRNAワクチンなどはそうしたワクワク感を追求した結果だ。そこでは「日本発」や「メードインジャパン」などにこだわることはあまり意味を持たない(図4)。
図4 特許とCOIの問題を解消して大学はもっとゴッソリ収益を上げるべき
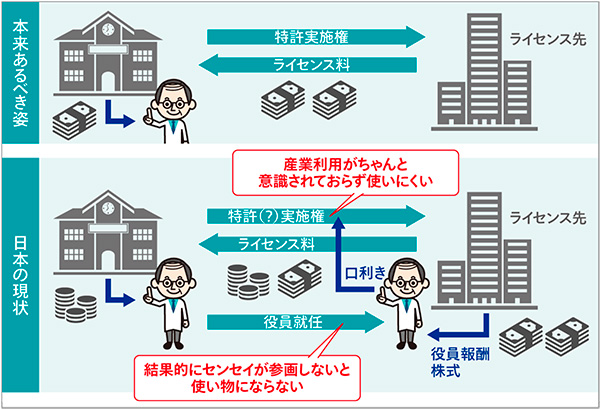
日本のベンチャーの課題としては、まず大学の手離れの悪さが挙げられる。日本の大学には全能感のようなものがあり、製品開発のようなものまで何でもできるという意識があるが、大学の研究は領域を広げるものであるのに対し、開発は領域を絞り込むものであって、そもそもマインドセットが違う。大学は研究を進めたら、あとは企業の得意な分野に手離れ良くバトンタッチしていくことが大切だ。またベンチャーの育て方も大事にしすぎではないかと気になる。ベンチャーは雑草のようなもので、ある程度環境を整えたら、あとは育つも枯れるも放っておくくらいがちょうどいい。
■セッション
失敗許容し、走り続ける文化を
ケイエスピー 代表取締役社長/ペプチドリーム創業者 窪田 規一 氏
日本のベンチャーエコシステムについて、ベンチャー経営者としての経験と現在のインキュベーターとしての立場から指摘と提言をしたい。
3つの課題がある。ベンチャーは大学などの研究機関と大企業との共同研究の形から生まれることが多いが、そこから誕生した知財の扱い方に、まず問題が起きがちだ。特許は両者で共同出願することが一般的だが、そのライセンスの利用には全共有者の了解を取らねばならず、大学などだけでベンチャーを立ち上げることはできない。国内ではこのような共同研究の知財の約60%が塩漬けになっているという統計もある。ベンチャー立ち上げの足かせにならないよう、大学などに単独出願を認めることが必要だ。一方、企業にはベンチャーに対してのビジネス優先交渉権を付与するなどすれば、知財がうまく回りだすだろう。

次にいざベンチャーを立ち上げ、エンジェルやベンチャーキャピタルなどからの出資を得ようというとき、そうしたことに長けた経営者の絶対数が少ない点だ。特に技術系ベンチャーには経営者人材が不足している。こうしたケースにはベンチャー経営を経験した人間、特にかつて失敗した経営者の活用を提言したい。わが国では失敗を許容する文化の不足が言われるが、「失敗から得られることは数多くあるものの、成功から得られるものは少ない」という格言に注目すべき時ではないかと思う。
3つ目は大企業との連携時におけるスピード感の欠如という問題だ。ベンチャーにとってスピードこそが命であり、瞬時の経営判断ができなければ成長は阻害される。過去の因習にとらわれたような仕組み、例えば大企業にありがちな稟議(りんぎ)書のような責任を分散させる仕組みは排し、意思決定システムを単純化、かつ一本化すべきだ(図5)。
図5
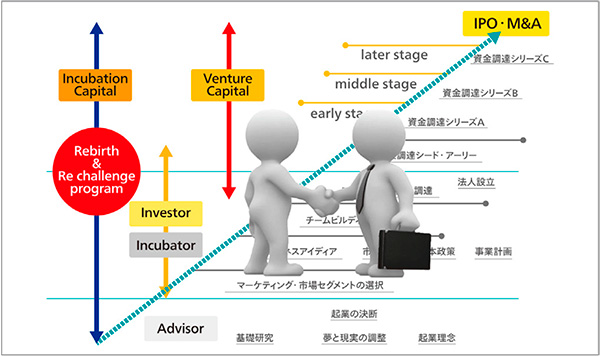
「この国の未来のために、孫子の世代に美田を残す」。これはインキュベーターとしての私たちのスローガンだ。そのために10年後、20年後の日本の基幹産業の芽を育てなければならず、ベンチャーがその役割を担うだろう。例えば米国ではナノパーティクルピルやエレクトリック・ヘルスレコードなど社会を大きく変えるようなディープテックが大手製薬業界と結びつき、すでに動き出している。日本の製薬業界でもベンチャーの力を生かし、ライフサイエンスとディープテックの組み合わせを加速させ、新たな基幹産業として育てていくべきだ。
■講演(4)
成功に導く アカデミアによる橋渡し
筑波大学 医学医療系 教授/つくば臨床医学研究開発機構 TR推進・教育センター長 小栁 智義 氏
過去30年間ほどで製薬業界の開発環境にどのような変化が起きたのか。創薬のコストが非常に増大したため、探索研究から非臨床などのアーリーステージは大学やベンチャーに任せ、そして企業は臨床試験に特化するなどのエコシステムが構築された。欧米では、こうした技術移転によるマーケットが形成され、世界市場での競争力が形成されたが、日本ではベンチャーがそうした力を持つことはほとんどなかった。では何が足りなかったのか。

米・スタンフォード大学のモシー・ローゼン教授は体内のとある酵素の研究から心筋梗塞の治療薬のアイデアを得た。彼女は手帳の裏に書き付けたアイデアをあらゆる人に見せ、最終的にVCから約30億円を調達した。その過程で彼女が学んだことは、研究成果が患者にとってどんなメリットがあるか、つまりゴールを明確に示すことの重要さだ。資金調達の問題点はここにある。大学の研究者たちが考えているアイデアを、最終的に製薬企業が薬にする。その間の過程でどういうデータを取り、どういう経済構造を持って開発を進めていくのか、その橋渡しをいかにスムーズにできるかだ(図6)。
図6 製薬業に必要とされている視点
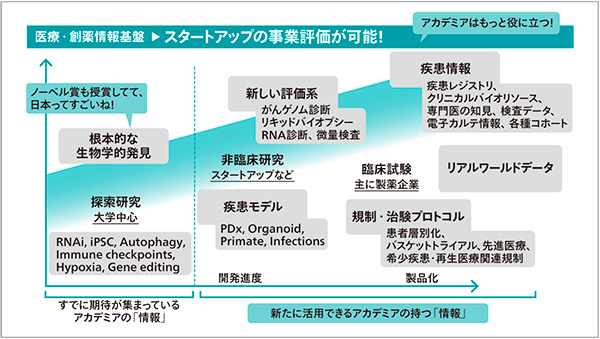
この学びはスタンフォード大学でトレーニングプログラム化され、世界で70以上の研究機関が利用している。日本では筑波大学でこのプログラムを実施し、臨床開発、薬事規制、知的財産、投資などといった様々な側面から研究者を教育しており、導入4年で治験に入るケースも出てきた。
日本のスタートアップやベンチャー企業に足りなかったのは、開始時点で最終製品をイメージした計画の立案だ。研究から生まれたシーズをどう製品化し、患者にどうやって届けるかというところまでを、ベンチャー企業が事業計画の中に細かく入れ込んでいくことができていなかった。また、同様に日本のベンチャー企業は、最初からグローバル市場で何が売れるかを明確にイメージして、モノをつくろうという姿勢にも欠けていた。
今後、創薬のスタイルというものは大きく変化してくだろう。膨大なデータをどう生かしていくかが鍵になり、グーグルやアマゾンといったIT大手が競争相手となってくる可能性もある。その時に製薬業界でのデジタルトランスフォーメーション(DX)の進展が大きな意味を持つ。アカデミアには、研究成果だけでなく、疾患情報や臨床情報などリアルワールドデータが豊富にある。DXを進めアカデミアとの情報流通のインフラを強固に構築することが今後協業を進める上において大切となるだろう。
■講演(5)
創薬ベンチャー育成 強化戦略推進
経済産業省 商務・サービスグループ 生物化学産業課長 佐伯 耕三 氏
コロナ禍において、主なワクチンを全量輸入に頼らざるを得なかったことは日本の創薬が置かれた状況を象徴的に示した。ファイザーのmRNAワクチンを開発したのはドイツのビオンテックというベンチャーであり、米国のモデルナもベンチャー、mRNAという新しい技術自体もベンチャーの中から出てきたものだ。いまや世界の医薬品開発数の約80%はベンチャーによるものであり、日本の創薬におけるベンチャーの育成やベンチャーエコシステム強化の立ち遅れという問題があらわになった。

一方、創薬ベンチャーには特徴的な課題がある。まず初期的な探索から薬事承認にいたるまで、一般的に10年以上の時間がかかる点。また臨床試験の初期の段階であっても、数十億円規模の資金がかかる点。そして治験までに候補薬がかなり選別されるうえに、治験の段階でも有効性や安全性の観点からも選別されるため、最終的な成功率が何万分の1程度とかなり低いという特徴もある。
そこで国は創薬ベンチャーエコシステム強化事業をスタートした。経営に特化した人材や薬事プロセス、知財戦略のプロなど多彩な人材をコーディネートできる能力など、創薬の特性を十分に理解し、ベンチャーを育成するハンズオン(成長支援)能力の高いVCをまず認定する。結果を出せるまで時間も資金もかかる創薬VCには能力ある人材が特に必須となる。そして、認定VCが10億円出資するのであれば国の補助金として20億円まで出資、合計すると30億円というレバレッジを効かせられる制度だ。こうすることで、創薬ベンチャーの資金調達を支えていく(図7)。
図7 創薬ベンチャーエコシステムの底上げに向けて
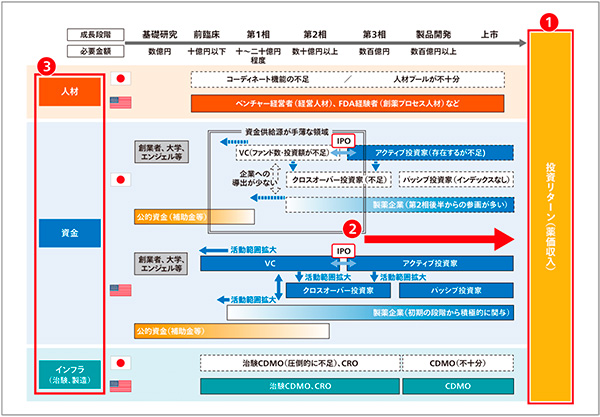
インフラ面においても創薬ベンチャーをめぐる状況は厳しい。例えば治験薬をつくりたいときに小ロットをつくれるような設備が国内には十分ではない。そうした治験薬の製造拠点や欧米に偏りがちな医薬品受託製造(CDMO)拠点の国内整備も支援したい。
エコシステムを回す血液は、投資に対するリターンだ。しっかりしたリターンが投資の前提であり、人材確保やインフラ整備が進む前提でもある。投資へのリターンを大きくするにはビジネスにおいて国内だけに目を向けるのではなく、海外の成長マーケットをしっかり確保する視点が必要だ。
最初から海外展開を想定する発想が求められる。今回の事業では、グローバル展開を支援できる能力を持つVCを認定し、海外での治験費用も補助の対象とする。さらに出口での製薬企業とのつながりも強めることで、エコシステムの構築につなげたい。
■講演(6)
世界とつながるイノベーション創出環境の整備を
日本製薬工業協会 岡田 安史 会長
新型コロナウイルス感染症のワクチン開発では、日本の製薬企業は大きく遅れを取り、日本のイノベーション創出力を懸念する声が相次いだ。
日本の製薬企業は数々の画期的新薬を創出してきており、現在でも世界有数の新薬創出国であることは間違いない。しかし世の中の様々な環境変化と同様に製薬産業を取り巻く状況やビジネスモデルも大きく変化している。製薬産業はこれまで垂直統合型が主流だった。つまり上流の研究開発から、下流の製造、販売に至るまでのバリューチェーンをすべて内製化するという自前主義だったが、今や水平分業型へと大きく変化している。バリューチェーンの各ステージは高度・複雑化しており、すべてを自社保有するのではなく、各ステージで自社にはない強みを保有する企業などと連携することが不可欠となった。

とりわけ0から1を生み出す創薬研究において、近年の創薬シーズの源泉について、その多くはベンチャーやアカデミアの研究に由来している。製薬産業がイノベーションを創出するには、ベンチャー、アカデミアとつながるエコシステムの構築が不可欠である。
モダリティ、すなわち創薬技術や手法も多様・高度化しつつある。飛躍的な技術の進歩により、従来の低分子医薬品に加え、細胞医療、遺伝子治療、核酸医薬といった多様なモダリティが登場、これまでアプローチできなかった希少疾患、あるいは難病に対する薬剤の開発も可能となった。これら新たなモダリティの起源も多くがベンチャー、アカデミアだ(図8)。
一方、日本のイノベーション創出力は国際比較において低下しつつある。指標の一つとなる引用論文数ランキングでは、この20年で日本は世界5位から10位へと順位を下げた。イノベーション人材の創出と国際化に必要な海外留学という観点からみても、米国大学の出身国別留学生数において、中国、インド、韓国からの留学生数が大きく伸びている半面、日本人留学生数は少ない。また、世界と比較して日本では起業を計画する人が絶対的に少ない。
図8 ヘルスケアイノベーション創出環境の変化
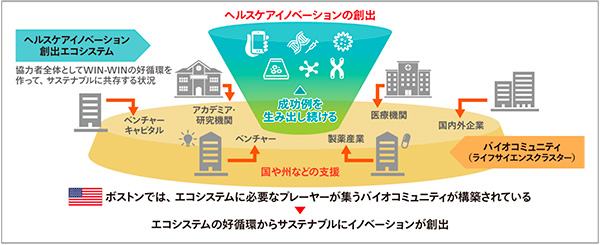
イノベーション創出には、それを支える資金も重要だ。とりわけ創薬には15年前後の時間、数百億から1千億を超える投資、2.5万分の1程度の成功確率という高いハードルがある。しかし、日本ではベンチャーキャピタル投資のGDP比率などで欧米に比べ大きな差があり、特に臨床の早期にかけての資金供給が不足している。前途有望なシーズがあっても先立つものがないという状況だ。こうした状況の打破に向けて、エコシステムの強化、イノベーション人材の育成や失敗を恐れない風土づくりなど、長期視点で考えうるすべてに着手すべきだ。
まず、有望なシーズを持つベンチャーやアカデミアと、シーズの実用化に必要な臨床試験実施や原薬製造能力を有する企業とのマッチングの推進が必要だろう。そのためには産業界がベンチャーやアカデミアに対してニーズをしっかりと伝えねばならず、対話が非常に重要だ。研究早期の段階から、アカデミアと産業界がコンソーシアムのような形で一体となって有望なシーズを発掘し磨き上げていくことも、解決策の1つになると考える。
次に人材育成について。世界では顕著な功績をあげ、強力な人的ネットワークをもつ優秀な人材に世界の投資家から莫大な資金が集まるという時代になりつつある。そうした人材の育成のためには、国家を挙げて若手研究者を支援し日本の研究力を高めるとともに、起業家精神旺盛で野心的な人材を次々と生み出す教育システムに変えていく必要があり、政府が掲げる新しい資本主義の成長戦略の柱の一つである10兆円大学ファンドには大いに期待している。
そしてベンチャー起業の活性化には、ベンチャーが学生にとって憧れの職業となることが不可欠であり、成功例を生み出すことが重要だ。昨年末に措置された創薬ベンチャーエコシステム強化事業の補正予算500億円を活用して成功例を生み出すことに、製薬企業としても早期のステージから積極的に関わり、世界とつながるエコシステムからのイノベーション創出を全力で支援していきたい。

