トピックス 「日本・中国ICH合同シンポジウム」を開催
2021年6月18日、厚生労働省、独立行政法人医薬品医療機器総合機構(PMDA)、中国国家医療製品局(NMPA)、および製薬協の共催により、「日本・中国ICH合同シンポジウム」をオンラインにて開催しました。
はじめに
2017年の中国の医薬品規制調和国際会議(ICH)加盟後、中国国内におけるICHガイドラインの実装が加速しております。今後、ICHガイドラインと中国国内規制のいっそうの調和が望まれることから、今般、日中双方のガイドライン実装状況および取り組みの共有、ICHガイドライン実装の加速、ICHに関する日中両国の協力の深化を目的として、日中2国間としては初となるICH合同シンポジウムを行いました。
シンポジウムの概要
当日は、両国のICHコーディネーターによる2021年6月上旬のICH仁川会議の結果報告に加え、ICHにおける日中協力のパネルディスカッション、Eトピック(臨床試験)最新動向、リアルワールドデータ最新動向、Qトピック(品質)最新動向、細胞治療・再生医療等製品の実情に関して、日中両国の規制当局ならびに産業界から講演がありました。
仁川会議結果報告において、中国当局からは、最終化されたトピックの中国国内の施行は、即時の場合もあれば、半年~1年間の経過期間を設ける場合もあり、今後も双方の規制当局の対話を強化し、アジア地域のICHガイドライン実装に力を入れたい、とのコメントが寄せられました。
また、パネルディスカッションでは、中国国家医療製品局(NMPA)から、「ICHガイドラインの内容が中国国内の規制に合わず、実装が難しい場合もあり、今後、海外の状況を学び、実装していきたい」との発言があり、製薬協からは継続的なICHガイドライン実装への取り組みおよび実装の妨げとなるローカルガイドラインの廃止検討等を要望しました。
終わりに
シンポジウム終了後、参加者からは、ICH創設メンバーとして厚生労働省・独立行政法人医薬品医療機器総合機構(PMDA)および製薬協の存在感が示され、本シンポジウムをきっかけとして、今後日中双方のICHにおける協力関係の、よりいっそうの深化を期待する声が寄せられました。
なお、当日のプログラムは以下の通りです(表1)。
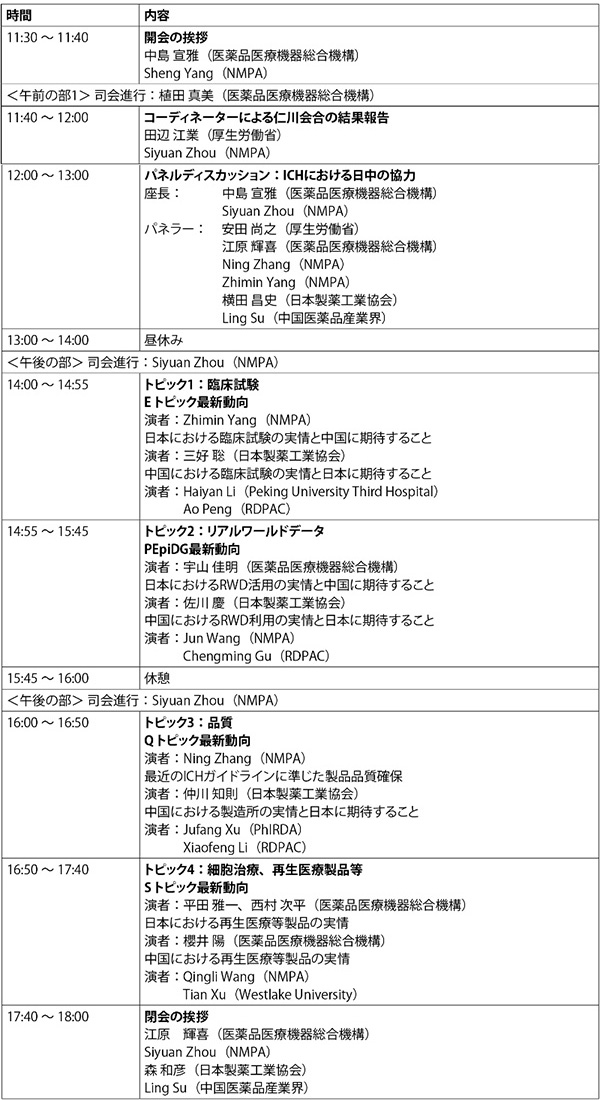 表1 プログラム
表1 プログラム
最後に、今回、初の試みとなる日中ICH合同シンポジウムの開催にあたり、ご尽力いただいた関係者のみなさんに、この場をお借りして改めてお礼を申し上げます。
(ICHプロジェクト、国際委員会 アジア部会 中国チーム)

