「製薬協メディアフォーラム」を開催 “日本版EHDS”実現に向けた現状と課題-次世代医療の実現に向けて-
2026年03月18日
2026年3月18日、室町三井ホール&カンファレンス(東京都中央区)にて「製薬協メディアフォーラム」を開催しました。今回は「“日本版EHDS”実現に向けた現状と課題-次世代医療の実現に向けて-」をテーマに、製薬協産業政策委員会の安中良輔委員、医薬産業政策研究所の渡邉奈都子主任研究員、東京大学名誉教授/一般社団法人次世代基盤政策研究所代表理事の森田朗氏による講演を実施しました。当日は会場およびウェブ配信にて、メディアや会員会社含め70名以上が参加しました。

フォーラム開催の背景
国民一人ひとりが最適な医療を受けることができる環境づくり、社会保障制度の持続性確保、革新的な新薬創出等に必要不可欠な医療DXの推進には、健康医療データの利活用が重要となります。2025年12月の医療法等改正法の成立を受け、医療情報の二次利用の推進に向けた取り組みの前進に期待される一方、まだ解決すべき課題は存在しており、解決までの道筋は決して平坦ではありません。本フォーラムでは、日本版EHDS(European Health Data Space)※の実現に向けた現状と課題について、内閣府の「医療等情報の利活用の推進に関する検討会」構成員の安中委員、森田氏による講演に加え、政策研が実施した「健康医療情報の利活用に関する国民意識調査」の結果の概要に関する講演を実施しました。以下は、講演内容の採録になります。
-
※EHDS:欧州における健康医療データ利活用の基盤となる政策
講演1
医療等情報の利活用の推進に関する検討会における議論と今後の課題
製薬協 産業政策委員会 健康医療データ政策GL 安中 良輔 委員
製薬企業は、健康医療データを用いた効率的な創薬を通じ、患者さんにいち早く革新的な医薬品をお届けしたいと考えています。しかし、製薬企業のためだけに悉皆性の高いデータベースを構築していただくことは、多忙な医療現場の負担を考えると現実的ではありません。理想とするのは、患者さんの健康増進や治療に用いられる「一次利用」で生まれたデータを、行政の医療コスト効率化や私たちのような製薬企業・アカデミアの研究開発といった「二次利用」にも役立てる一体型のグランドデザインです。

製薬企業は、健康医療データを用いた効率的な創薬を通じ、患者さんにいち早く革新的な医薬品をお届けしたいと考えています。しかし、製薬企業のためだけに悉皆性の高いデータベースを構築していただくことは、多忙な医療現場の負担を考えると現実的ではありません。理想とするのは、患者さんの健康増進や治療に用いられる「一次利用」で生まれたデータを、行政の医療コスト効率化や私たちのような製薬企業・アカデミアの研究開発といった「二次利用」にも役立てる一体型のグランドデザインです。
医療データを利用することで、製薬企業が国民の皆様にご提供できるメリットは主に3つあります。1つ目は、副作用のリスク低減です。大規模な医療データをもとにリアルタイムで医薬品の安全性情報を分析し、適正使用に繋げることが最も大事なことだと認識しています。2つ目は、研究開発に利用することで新薬をお届けできるまでの期間が短縮されることです。そして3つ目は、ゲノムデータなどの活用や研究計画の質の向上により臨床開発の失敗が減り、新薬が生まれる成功確率が高まることです。
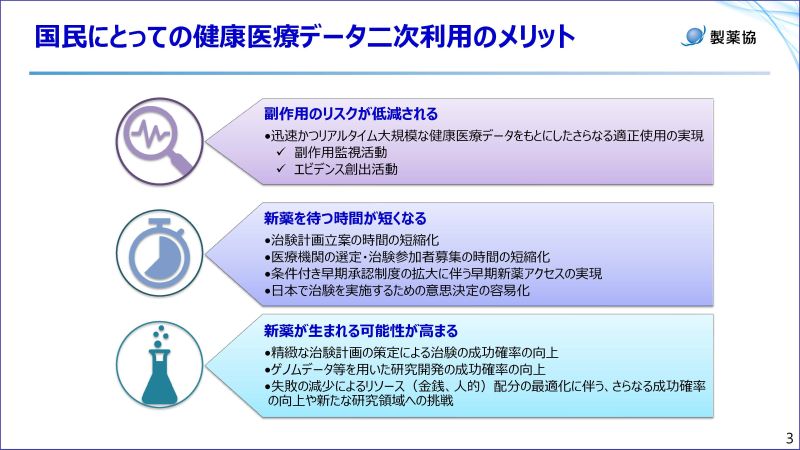
具体的には、治験の対照群の一部または全部を医療データで保管することで、データ収集の効率化を行うニーズがあります。また、たとえば発がん性といった長期間経たないと現れない副作用の追跡ニーズや、遺伝性疾患の研究には親子間のデータ連携のニーズもあります。そのためには、日本が世界に誇る母子手帳や学校健診など、生まれる前から亡くなるまでのデータが繋がる「ライフコースデータ」の基盤構築が必要です。

厚生労働省は現在、全国医療情報プラットフォームを構築しようとしており、医療や介護、自治体のデータを連携させて、よりよい医療を患者さんに提供することを目指しています。直近では、昨年12月に成立した医療法等改正により、3年後を目途に厚労省が保有する公的データベースが、仮名化・匿名化した安全な状態で二次利用できるようになります。2030年末までにクラウドベースの電子カルテの普及率100%を目指す内容も盛り込まれ、非常に心強く感じています。
この新たな基盤では、ナショナルデータベース(NDB)を中心に、さまざまなデータベースが連携可能になります。特に注目すべきはさまざまな医療データと「死亡データ」が連結解析可能となるなる点です。有効性を評価する上でも、副作用として一番重い事象を分析する意味でも、製薬企業が最も必要としていたのがこの死亡データであり、これまでは民間のデータベースからも十分に入手できませんでした。
また、不正利用を防ぐ面でも非常に高い仕組みが設計されています。利用者は、クラウド上でデータを解析することはできますが、個人情報である解析対象のデータのダウンロードはできません。解析した結果(非個人情報)だけを持ち出す仕組みとなっているため、個人情報が漏洩・流通することは構造上あり得ません。
これらのデータベースが単独ではなく「連携」して解析できるようになることの意義は計り知れません。たとえば、処方や死亡データが入ったNDBと、詳細な情報を持つ全国がん登録を連携させることで、抗がん剤投与後の全生存期間(OS)といった最も重要な評価が可能になります。また、予防接種データベースが拡充されれば、ワクチンの副作用や有効性評価もできるようになると期待しています。
日本でもデータベースの連携を進めていくうえで、ヨーロッパの「EHDS」は本当に素晴らしいモデルです。日本政府も2025年の閣議決定で、EHDSを参考にした検討を行い、来年の通常国会での法案提出を目指すという不退転の決意を示されました。これを受け、森田氏が座長を務める新たな検討会が立ち上がっており、製薬協も真摯に検討会に臨んでまいります。
この制度設計に向けて、私たちが特に強調している点が2つあります。1つ目は、データの構造化に対する「生成AI(大規模言語モデル(LLM))」の活用です。データ構造化がなかなか進まない現状に対し、AIの活用も両睨みで検討すべきです。実際に、抗がん剤投与後の腫瘍サイズの変化において「人が評価した結果」と「AIが評価した結果」がほぼ一致したという事例も出ており、AIも十分活用できることが示唆されています。
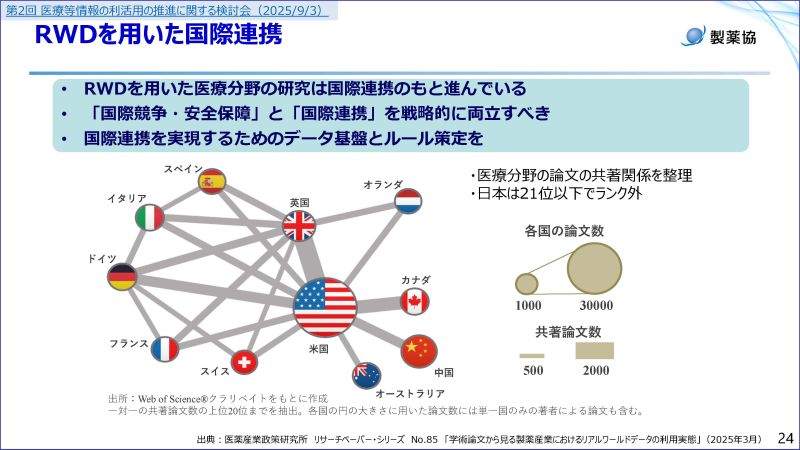
2つ目は、「国際連携」です。医療分野の研究開発は、もはや国際連携なくしては成立しません。現在、経済安全保障の観点が非常に重要になっていますが、実際のリアルワールドデータ(RWD)を用いた論文数を見ると、米国と中国の間でもしっかりと連携がなされています。日本も安全保障と国際連携を両立させ、海外と連携できる国際標準でのルール策定を進めるべきだと考えています。
講演2
健康医療情報の利活用に関する国民意識調査の結果概要
政策研 渡邉 奈都子 主任研究員
健康医療データの利活用を進めるためには、ライフコースデータ基盤の構築や法制度の整備に加えて、「国民の皆様の理解と信頼に基づく社会的受容」が不可欠です。本調査ではこの「社会的受容」に焦点を当て、国民の皆様の意識構造について分析を行いました。
先行研究を整理すると、健康医療情報の利活用に対する受容意識は、大きく5つの要因から構成されると考えられます。具体的には「個人の属性的背景」、理解・判断を支える「前提条件」、「利活用への動機」、「懸念」、そして「利活用主体への信頼」です。

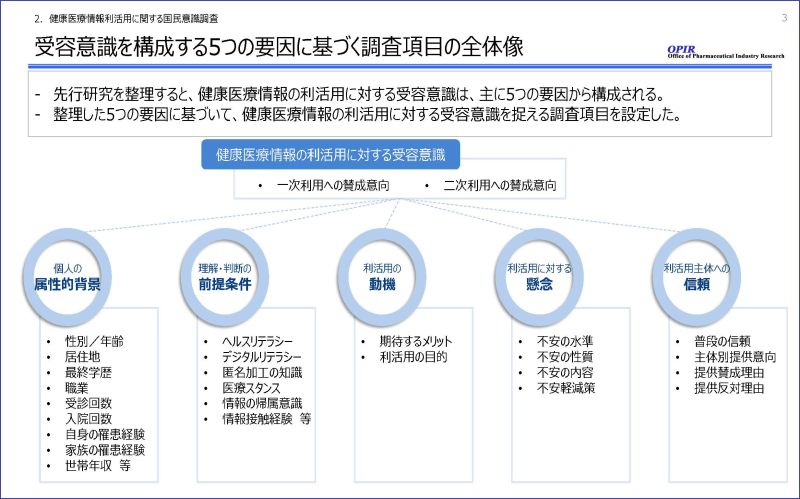
今回はこの5つの観点に基づき、全国47都道府県の20歳以上の男女2,900名を対象に、日本の人口構成比に合わせて偏りが生じないようWebアンケート調査を実施しました。
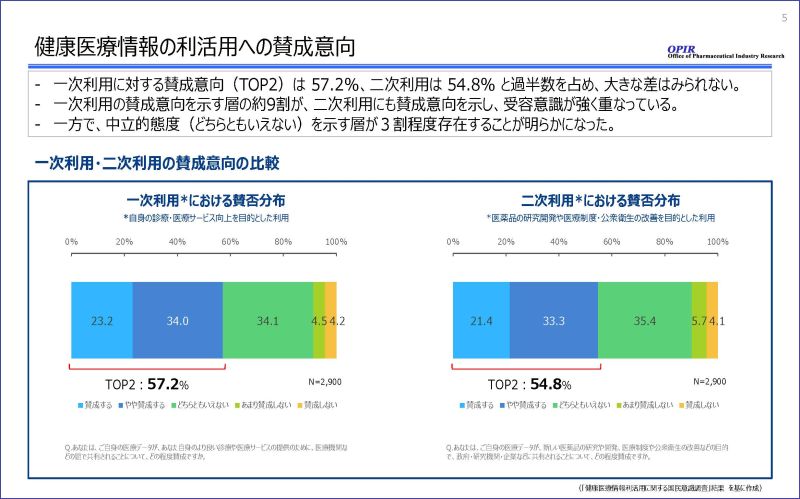
まず最も重要な結果ですが、自身の医療データが「自身の診療や医療サービス向上」のために使われる「一次利用」に対する賛成意向は57.2%、そして「新しい医薬品の研究開発や公衆衛生の改善」などを目的とした「二次利用」に対する賛成意向は54.8%でした。いずれも過半数を占め、一次利用と二次利用で受容意識に大きな差は見られませんでした。また、一次利用の賛成意向を示す層の約9割が、二次利用にも賛成意向を示し、受容意識が強く重なっています。一方で、約3割がどちらとも言えないと回答しており、明確な反対ではなく、判断を保留している層が一定数存在していることも明らかになりました。
この数値を国際比較で見ると、日本はフランスやイギリスと同水準の中位グループに位置するものの、経済協力開発機構(OECD)平均の64%は下回っています。
では、どのような要因が二次利用への賛成意向を高めているのでしょうか。分析の結果、最も強い影響を与えていたのは「期待するメリットの数が多いこと」でした。次いで「不安や抵抗感を感じないこと」、「利活用主体への普段からの信頼」、さらに「匿名加工の知識」や「ヘルスリテラシー及びデジタルリテラシーの高さ」といった前提条件も関連していました。
つまり、データ提供への賛成意向は固定的な価値観だけで決まるものではなく、メリットの理解や不安の払拭、知識の蓄積によって、後からでも十分に高めることが可能な側面を持っています。
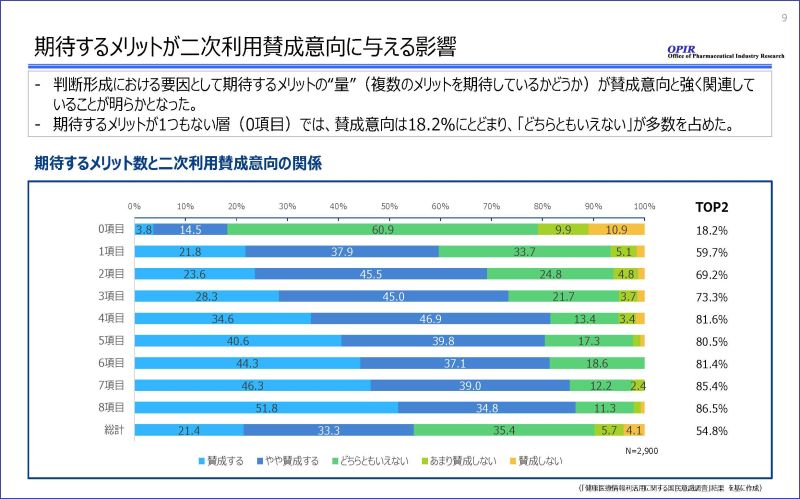
メリットの中身をさらに深掘りすると、「自分や家族に合った医療が受けられる」といった個人的メリットと、「新薬や治療法の開発に繋がる」といった社会的メリットの、両方を同時に重視する層が最も多いことがわかりました。また、メリットを一つも感じていない層の賛成意向は約18%にとどまりますが、4項目以上のメリットを期待している層では、8割以上が賛成しています。メリットを多く認識するほど、賛成意向が段階的に高まる傾向が明確に確認されました。
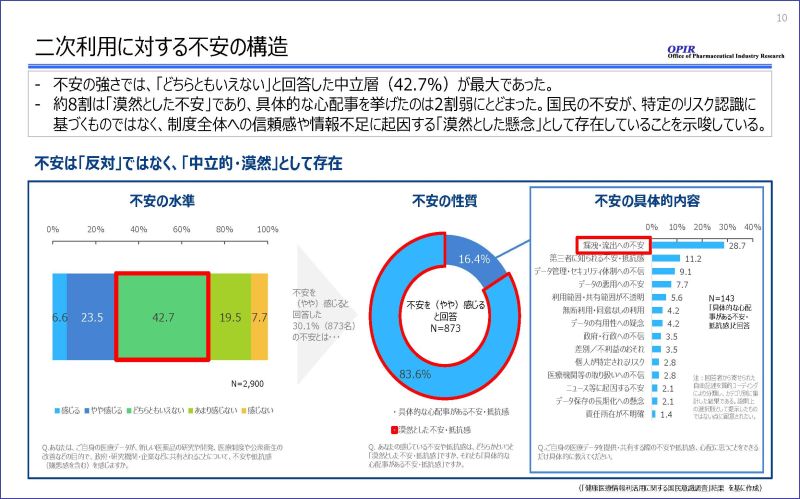
データ利活用に不安を感じる要因についても分析しました。そもそも強い不安を感じている層は3割に満たず、「どちらともいえない」とする層が42.7%で最多でした。さらに注目すべきは、不安を感じている人のうち「具体的な心配事がある」と回答した方は2割弱に過ぎず、約8割は「漠然とした不安」を抱えているという点です。これは、国民の皆様の不安の正体が、何か特定のリスクに対するものというよりも、情報不足や制度全体への信頼感に起因する漠然とした懸念であることを示唆しています。
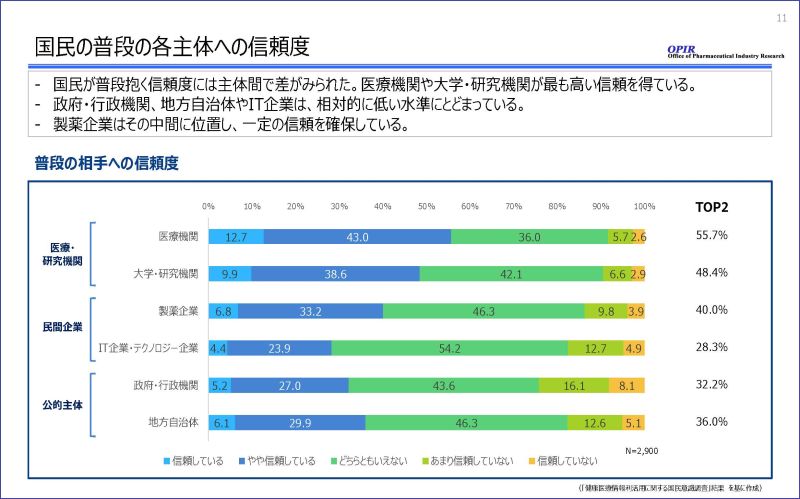
最後に、利活用主体に対する信頼度についてです。結果として、医療機関や大学・研究機関が最も高い信頼を得ている一方、政府・行政機関やIT企業は相対的に低い水準にとどまり、私たち製薬企業はその中間に位置していました。
データを提供してもよいと判断した理由を聞くと、行政に対しては「公共性」、医療機関や製薬企業に対しては「専門性」が挙げられました。反対に提供を拒否する理由としては、製薬企業やIT企業に対しては「営利性への懸念」、行政に対しては「透明性・説明責任の不足」が中心でした。そして、すべての主体に共通していたのが「プライバシー保護への不安」です。この結果は、データの受け手側が「どのような目的で、どうデータを扱い、どうプライバシーを守るのか」を踏まえた透明性のあるガバナンス設計が不可欠であることを示しています。
本調査を通じて、一定割合の国民が明確な賛否を示さない「どちらともいえない」状態にあることがわかりました。この層は決して強い反対意識を持っているわけではなく、判断に必要な情報が不足している、あるいは関心がまだ高くない状態だと考えられます。受容意識を向上させるためには、こうした態度保留層の方々に向けた関心の喚起と、利活用の意義や価値に対する具体的な理解の促進が重要です。
講演3
日本版EHDS実現に向けた現状と課題
東京大学 名誉教授/一般社団法人次世代基盤政策研究所 代表理事 森田 朗 氏
コロナ禍において、日本ではFAXでの情報集約が話題となりましたが、データを集めて使うことに関して欧米から大きく遅れていることが痛感されました。これからデジタル化を進める以上、日本もデータ利活用を加速していかなければなりません。
ヘルスデータを活用することで、私たちが病気になった際に「個別最適化された治療(一次利用)」が可能になります。たとえば、初めての病院で過去の病歴や服薬歴を聞かれても、10年、20年前のことは正確に覚えていません。しかし、データが繋がっていれば、医師は正確な情報に基づき、ゲノム情報等も加味したうえで、その人に最も有効な治療法を早く提供することができます。

そして、本日の主題である「二次利用」は、全国民の健康医療データを集めて分析し、「こういうタイプの人にはこの薬が効く、あるいはリスクがある」といったことを統計的に明らかにし、創薬や医学研究、さらには最適な医療政策に役立てるものです。
そのためには、出生から死亡までの健康状態を記録する「ライフログ」の保存が重要です。この健康状態を記録しておけば、病気が発症する「閾値」に達する前の状態を見つけ出し、発症を遅らせる予防医療も可能になります。
しかし、データを繋ぐには、フォーマットが揃っていること(標準化)と、確実な本人確認ができる共通の「識別子(ID)」が必要です。日本には母子手帳や学校健診など世界に誇るデータがありますが、行政の各部門がそれぞれの目的で部分最適にシステムを作ってしまったため、データが標準化されておらず繋がりません。さらに、個人の権利保護の方法として「同意」や「匿名化」にこだわりすぎた個人情報保護が、データ利活用を妨げてきました。つまり日本には、医療情報をどう使い、どう結びつけるかという全体としての「グランドデザイン」が欠如していたのです。
こうした遅れに対する危機感から、2025年の「骨太方針」や規制改革実施計画等において、データ利用を促進する方針が強く打ち出されました。これを具体化するため、私が座長を務める「医療等情報の利活用の推進に関する検討会」がスタートし、今年の夏を目処に結論を出し、法案提出を目指しています。
この議論において、政府の閣議決定でも参照するモデルとされているのが、EUで2025年3月に発効した「EHDS規則」です。日本の閣議決定文書で、これほど明確に「外国の制度を参照しましょう」と書かれるのは珍しいことです。もちろん日本固有のものを作ることは重要ですが、良いものはしっかり踏まえて、それを参考にさらに良いものを作るべきだという期待の表れであり、EHDSはまさに参照に値する制度です。
そもそもEHDSがなぜできたのかというと、2020年からの新型コロナウイルスのパンデミックが契機です。パスポートなしで自由に行き来できるEU域内において、感染者もウイルスも国境を越えて移動するにもかかわらず、27のEU加盟国ごとに医療データの仕組みがバラバラでした。緊急事態として急遽システムを作って対応したものの、この苦い経験から「EU域内全体で感染状況を正確に把握し、データを使えるようにしなければならない」と痛感しました。同時に、「これだけデータが集まるなら、公衆衛生だけでなく、創薬や医療機器開発といった産業振興に結びつけない手はない」という狙いも持って作られました。EUでは現在、データを使って社会を動かしていく時代を見据え、「EU一般データ保護規則(GDPR)」や「AI法」といった分野横断法と、ヘルス、農業、環境など領域別の法律を組み合わせた壮大なマトリックス的法体系を作ろうとしています。
EHDSとは、誕生から死亡までのライフログを一人ひとりについて蓄積し、それを日々の健康管理や治療(一次利用)、医学研究や創薬(二次利用)に活用しようというものです。コアになるのは高度に標準化された安全な電子カルテ「EHR(Electronic Health Record)」です。このEHRの基準を満たした各国のデータベースを繋ぐプラットフォームとして、一次利用のための「MyHealth@EU」と、二次利用のための「HealthData@EU」が構築されています。
一次利用(MyHealth@EU)において最も重視されているのは、「患者がより良い医療を受ける権利」です。たとえば、スウェーデン人が旅行先のフランスで急病になった際、フランスの医師にスウェーデンの自分の電子カルテを見てもらい、最善の治療を要求することができます。自分の病歴を他国の医師に知られたくない場合は、データを見せないオプトアウトの権利も認められていますが、情報が欠落した結果、最適な治療が受けられなくても「それはあなたの責任ですよ」という仕組みになっています。このように、患者の利益を第一に考えたシステム設計がなされているのです。
「二次利用」については、非常に厳重で考え抜かれた仕組みが導入されています。鍵となるのは、各国に設置が義務付けられた「ヘルスデータアクセス機関(Health Data Access Bodies)」という窓口あるいは規制機関です。二次利用のプロセスは以下のようになります。
-
カタログ登録の義務
病院、医学研究者、製薬メーカーなど、データを持つ者は、自分がどんなデータを持っているかを「公的メタデータカタログ」に登録することが義務付けられます。
-
利用申請
医学研究者や製薬企業は、カタログを見て「この目的で、このデータを使わせてほしい」とアクセス機関に申請します。
-
審査とデータ収集
アクセス機関が利用目的や必要なデータの種類、量等を審査し、許可を出すと、データ保有者にお金を払ってデータを提出させます。
-
データセットの作成
アクセス機関がさまざまな所から集めたデータをIDで紐付けし、個人が特定できない仮名化・匿名化し加工された「データセット」を作成します。
-
セキュアな環境での解析
利用者は生データをダウンロードできません。リモートアクセスで外から入り、安全性を確認された解析ツールを使って解析を行います。
-
結果の持ち出しと破棄
統計的な解析結果だけを受け取り、用が済んだデータセットは消去されます。
これだけ厳格な手続きを経るからこそ、EU委員会は当初「二次利用に個別の同意は一切不要」と提案しました。しかし、議論の過程で「憲法上オプトアウトの権利が保障されている国がある」ことから、オプトアウトを全く必要としないデンマークやフィンランドなどは反対しましたが、最終的にはオプトアウトの権利が認められました。ただし、公共的な目的の調査や政策形成等については、オプトアウトの権利は、例外として認められていません。また、高度な数学的処理で個人識別をほぼ不可能にする「PETs(Privacy-Enhancing Technologies)」を活用することで、オプトアウトをしなくても個人情報が漏れるリスクを極小化する技術的アプローチも進められています。
なお、データは医学研究や創薬、公衆衛生、政策立案などに利用できますが、データを使って「差別」をしたり、ターゲティング等の「商品販売・広告」に使ったりすることは固く禁止されており、アクセス機関がこれを厳しく監視します。
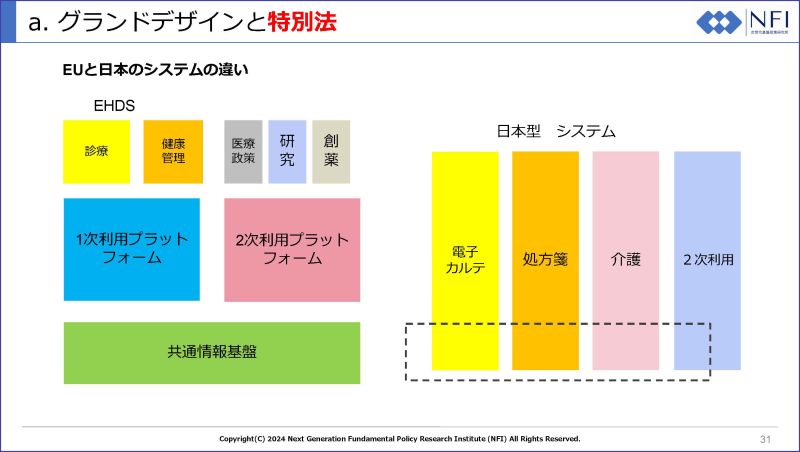
日本の現状を見ると、仕組みづくりにはいくつかの課題があります。まず、EUは「できる・できない」に関わらずトップダウンで決めて進めますが、日本は「確実にできる」と合意できてからスタートするため、どうしても歩みが遅くなりがちです。また、システム構造についても、EUが「共通の情報基盤の上にさまざまなアプリが乗る」形なのに対し、日本は行政の目的ごとの「縦割り」でシステムが作られており、それを後から共通基盤で繋ごうとしているため、非常に大変な作業になります。
そして、何と言っても「国民の信頼」が大切です。「営利企業である製薬メーカーに使わせていいのか」という漠然とした不安を持つ方々がまだいらっしゃいます。こうした方々に、データ利活用によるメリットと、安全を担保する厳格な仕組みを正しく説明し、信頼を獲得していくことが不可欠です。
 質疑応答の様子
質疑応答の様子
(広報委員会)

