Opinion 医薬品産業におけるCOVID-19パンデミックへの対応と今後
医薬産業政策研究所 統括研究員 村上直人
医薬産業政策研究所 主任研究員 鍵井英之
医薬産業政策研究所 主任研究員 澁口朋之
医薬産業政策研究所 主任研究員 枡田竜育
はじめに
新型コロナウイルス(SARS-CoV-2)による感染症(COVID-19)1)パンデミックは、ワクチンや抗ウイルス薬といった感染拡大抑止に有効な手段がない中、甚大な健康被害をもたらしており、いまだに収束の見通しが立っていない。他者との接触を極力避けることが現時点で最も効果的な感染防止策ではあるが、徹底し続ける代償としてリーマンショック後を凌ぐ社会的、経済的損失を世界中にもたらすこととなった。感染防止と社会的、経済的活動の活性化との適度なバランスの模索は、産学官民を問わず世界中の人々にとって正解のない難問となっているが、そのような中、国民の健康維持の一翼を担う医薬品産業は、その社会的使命を継続して果たすべく努力を重ねている2)。本稿では、当産業に対するCOVID-19の影響と、COVID-19の予防、治療薬の研究開発動向、そして将来起こり得る第2、第3の新興感染症パンデミックを想定した今後の取り組みについて述べてゆく。
1.産業活動に対する影響
(1) 業績に対する影響
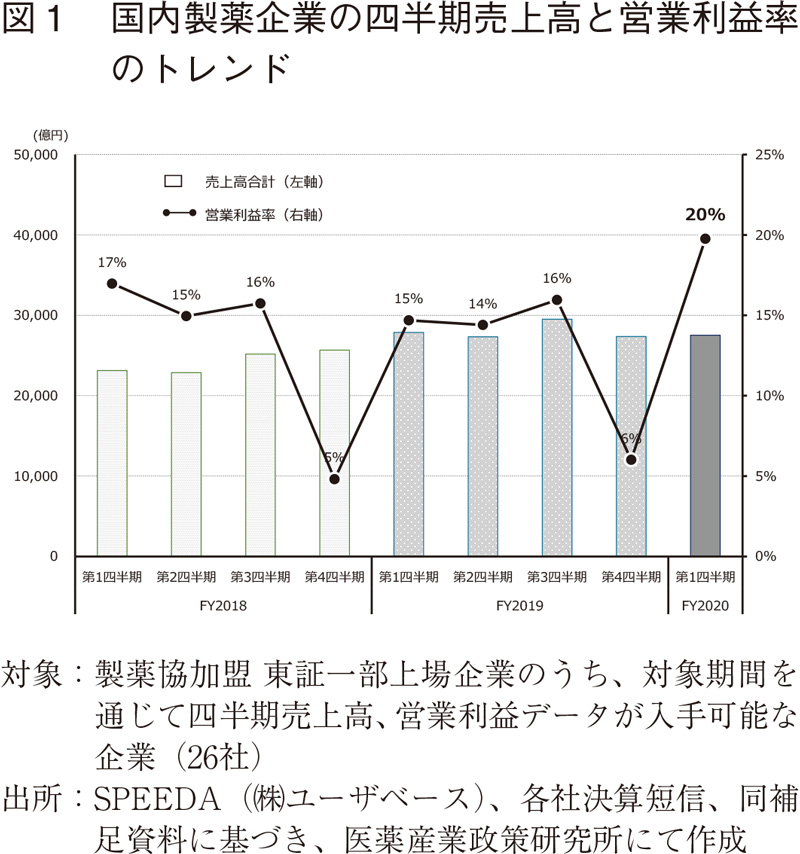
2020年度の国内医薬品市場は、2年毎に行われる診療報酬改定に伴う薬価改定により▲4.38%(医療費ベースでは0.99%)の圧縮が講じられたことに加えて、COVID-19に対する緊急事態宣言などに伴う患者の受診動向の抑制による影響が生じている3)。その中で、患者の受診抑制に伴い、品目によっては需要の減少によって売上高が減少しているケースもあるが、2020年1-3月期、4-6月期のいずれの連結決算報告(図1;研究開発志向型製薬企業を会員とする日本製薬工業協会(製薬協)の上場会員会社26社の集計)からも医薬品産業の売上高、営業利益は、他産業に比べると総じて堅調に推移していることが読み取れる。殊に営業利益については、各社の経営戦略に伴って各社各様であるが、全体としては、医薬情報提供活動など対外的な業務の自粛や研究開発活動の制限などによる販売管理費の抑制が寄与していると考えられる。
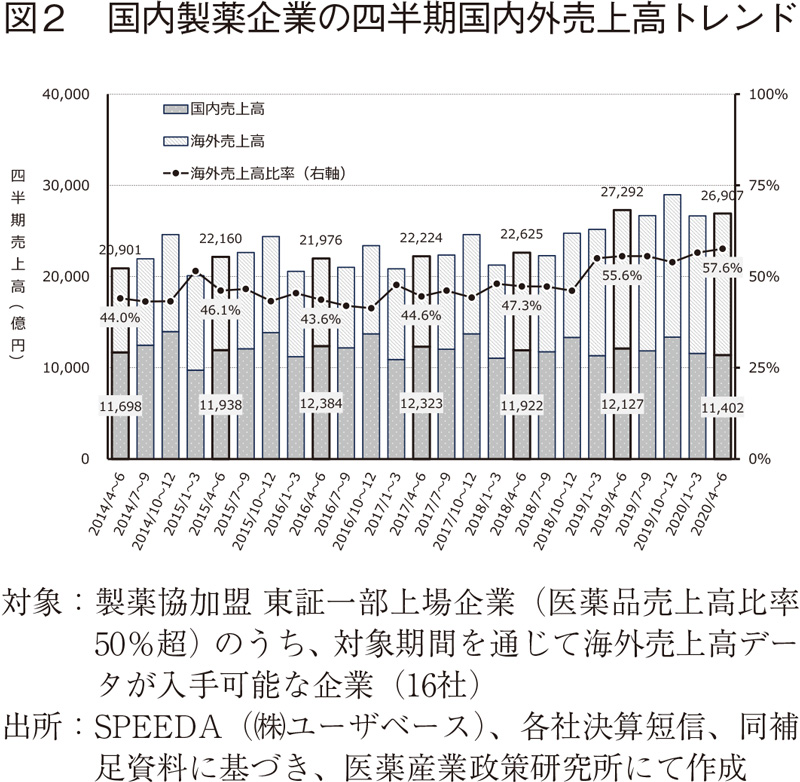
今後受診動向が回復基調に転ずるか否かなど、市場を取り巻く環境が不透明であることは言うまでもないが、4-6月期を経た段階に限れば、パンデミックに伴って業界全体として事業継続への深刻な影響を及ぼす業績へのインパクトはないように見受ける。更に連結売上高を構成する国内外売上高の推移を検討したが(26社のうち、医薬品事業の売上高が総売上高の50%超で調査期間中の海外売上高データが入手可能な16社を集計)、やはりCOVID-19パンデミックによる国内売上高に対する明確なネガティブインパクトは認められなかった(図2)。
(2) サプライチェーンに対する影響
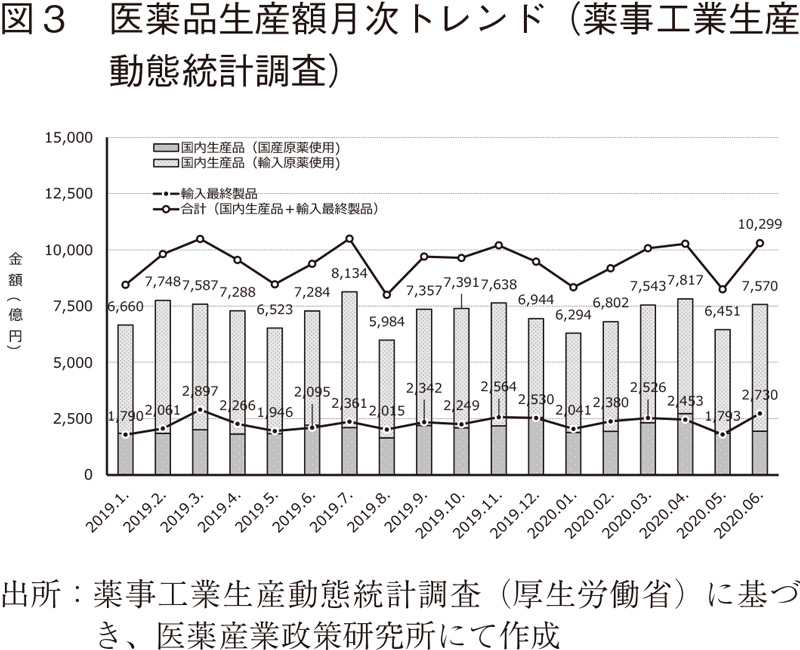
COVID-19が拡大する中、日本ではマスクや防護服といった医療物資の不足が大きな問題となった。また、医薬品の一部においても出荷制限がかかるなど供給不安の声があがった。医薬品のうち、医療用医薬品に関しても、その生産に必要な原薬等の調達先としていた海外で製造、輸出が滞ったために2020年5月末から7月末にかけて供給不安に陥る可能性のある製品は計14品目あったが、いずれも企業間での調整による欠品回避や、代替薬について各企業が学会と連携し、対応が図られている4)。医療用医薬品全体でみると、図3に示すように医薬品の国内生産額と医薬品の輸入金額の月次推移において世界で流行が進んだ2020年2月以降も2019年同月と比べて大きな変化は認められず、また、今年の5月から6月にかけて輸入原薬を使用した国内生産製品や輸入最終製品生産の着実な回復が窺われており、医療用医薬品の供給面でも、幸いにしてCOVID-19パンデミックによるネガティブインパクトは認められなかった。
医薬品の供給不安が回避された理由の一つに、先発品を中心に製品および製剤化前の原薬の在庫を製薬企業各社が6カ月分程度確保していたことが挙げられる5)。図3に示すように医薬品の生産に関しては輸入原薬使用を含め国内生産が全体の7~8割を占めており、製品のみならず原薬を確保しておくことで供給体制の安定化が図られてきた。2008年に新型インフルエンザのパンデミックに備え、製薬協から「製薬企業における業務継続のための新型インフルエンザ対策ガイダンス」が策定され6)、これをもとに各社の判断で重要と考えられる医薬品の在庫確保等を行ってきたことも安定供給の確保に寄与していると思われる。
(3) 臨床試験に対する影響
COVID-19の流行により、医療従事者の負担が増え、被験者の感染リスクが高まったことで、臨床開発にも影響が出ている。日本医師会が国内の臨床試験実施施設を対象にCOVID-19の影響について調査しており、一部の施設では、新規の治験の受け入れ中止、実施中の臨床試験の中断や新規の患者登録の中止等の対応が取られている7)。この傾向は世界的に同様であり、ニューヨークがん研究所とIQVIA社が2020年3~4月にかけて実施したアンケート調査によれば、がん領域の臨床試験に関して新型コロナウイルス流行前と比較して遅延もしくは中断されている施設の割合は米国80%、欧州86%、アジアでは40%とされている8)。このような臨床試験の遅延はCOVID-19パンデミック前に見込んでいた新薬の上市時期の遅れなどに繋がり、事業計画や中長期的な業績にも影響を及ぼす可能性がある。
2.COVID-19の予防、治療に向けた新薬の研究開発動向
COVID-19パンデミックに対応するため、世界各国の製薬企業を中心にCOVID-19関連の医薬品開発が急ピッチで進んでいる。医薬品の研究開発情報を収集しているBioCenturyの情報によると、2020年8月3日現在、世界各国で承認もしくは第Ⅰ相以降の臨床試験が実施されている化合物は治療薬243品目、ワクチン35品目となっている9)。グローバルで見ると、米国企業が開発スピードおよび数でリードしているが、国内でも多くの製薬企業10)に加え、バイオベンチャーやアカデミアがCOVID-19に対する治療薬、ワクチンの開発を進めている。一日も早くヒトにおける有効性、安全性を検証し、世界中で広く予防、治療に供することも医薬品産業の最大の使命であり、各社とも、最大限の努力を払っている。
(1) 治療薬
現在、国内でCOVID-19の適応で承認されている医薬品は、レムデシビル(ブランド名:ベクルリー)およびデキサメタゾンの2剤である。レムデシビルは元々エボラ出血熱の治療薬として米国ギリアド社が開発を進めていた薬剤であるが、COVID-19に対する治療効果が示唆されたことから、米国における緊急使用許可に基づく使用実績を踏まえて、2020年5月7日に国内で特例承認された。またデキサメタゾンは、古くから使用されているステロイド薬であり、重症感染症の適応を有するが、厚生労働省「新型コロナウイルス感染症診療の手引き」の中で「日本国内で承認されている医薬品」として掲載されている。
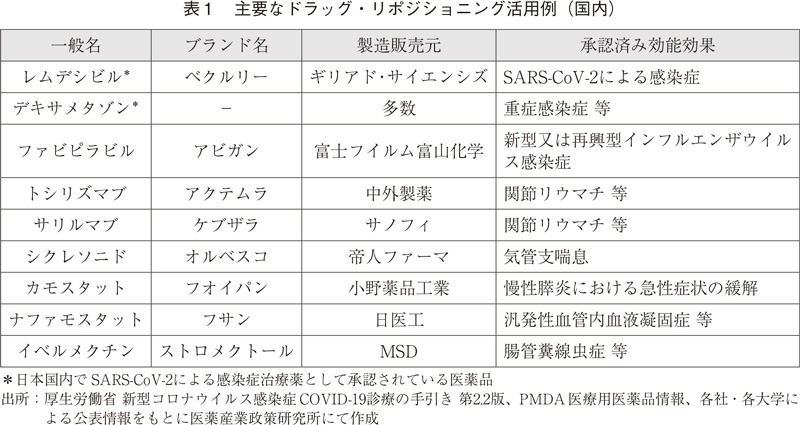
レムデシビルやデキサメタゾンのように、既にヒトでの使用実績がある薬剤を、本来の治療対象とする疾患以外の疾患の治療に転用する手法、所謂ドラッグ・リポジショニングが活用されている。国内における主要なドラッグ・リポジショニング活用例を表1に示すが、それぞれの既承認適応症や薬理作用が多岐にわたっており、COVID-19の臨床像の多様性と治療の困難さが窺われる。また理化学研究所と京都大学は共同で、世界最高水準の計算能力を有するスーパーコンピュータ"富岳"を活用し、既存薬2,128種の薬剤からSARS-CoV-2に効果を示すことが期待できる薬剤数十種類を選択(そのうち12種類は既にCOVID-19に関する臨床研究や臨床試験が実施中)することに成功したとの報道11)がなされおり、その後の評価の進展が期待されるところである。
既存薬の活用だけでなく、COVID-19治療を主目的とする新規医薬品の開発が国内製薬企業各社でも進められている。武田薬品工業(株)ではCOVID-19回復患者の血清から高度免疫グロブリン製剤(H-Ig)の開発を進めており、中外製薬(株)は、COVID-19に対する抗体医薬品の開発を進めている。こういった新規医薬品には高い有効性が期待されるものの、ドラッグ・リポジショニングに比べ特に安全性に関する検討が必要であり、実用化までにはより長期間を要すると思われる。
(2) ワクチン
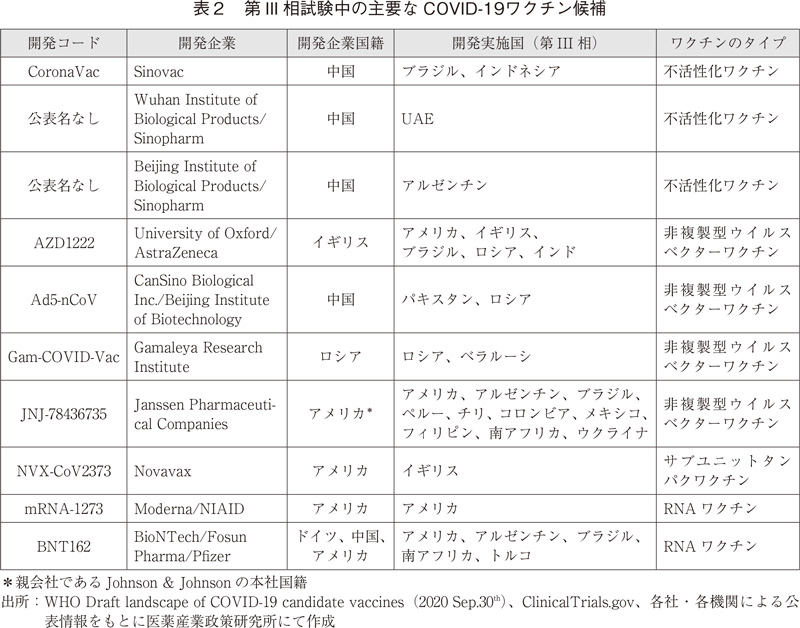
治療薬と並んで、あるいはそれ以上に感染や重症化の予防に有効なワクチンに対するニーズは高く、世界中で政府などからの強力な支援を受けて、多数の候補品の研究開発が進められている。表2に世界保健機関(WHO)の情報をもとに第Ⅲ相段階にあるとされている品目をまとめた。
国内企業によるワクチン開発では、第一三共(株)(RNAワクチン;DS-5670)、田辺三菱製薬(株)(植物由来ウイルス様粒子を活用したワクチン;MT-2766)、塩野義製薬(株)(遺伝子組み換えワクチン)など大手製薬企業だけでなく、バイオベンチャー企業であるアンジェス(株)が自社創製したDNAワクチンの臨床試験(第Ⅰ/Ⅱ相)を実施しているなど、ワクチンの研究開発や技術ノウハウを有する企業やアカデミアなど様々なプレイヤーが協力し合いSARS-CoV-2に対するワクチンの研究開発を進めている。
欧米諸国を中心に海外では社会、経済活動の本格的な再開を目指してかなり前のめりに規制緩和、解除を試みているが、より積極的に推進した国々の中には再び感染者数が増加し始める事態に陥っており、ワクチン接種開始への期待が非常に高まっている。ワクチンでは健常者が投与対象となるため、投与によるリスクとベネフィットの評価を、患者が投与対象となる治療薬に比べてより厳格かつ客観的に進める必要がある。早期開発成功への大きな期待とプレッシャーがかかるなか、欧米製薬企業9社が実施中のワクチン開発に対し、安全を最優先し、効果が確認されるまでは当局に承認を求めないとの共同声明を発表して、医薬品産業の生命関連産業としての矜持を示したことは特筆に値する。
3.将来への備えのために
米国では2020年4~6月期の実質GDP(国内総生産、季節調整済み、速報値)が年率換算で前同期比32.9%減となり、これは1932年の大恐慌時を超える歴史的な落ち込みと伝えられ、また、本邦でも同様に27.8%減(年率換算、物価変動調整済み、速報値)と報じられているように、COVID-19パンデミックに伴う景気悪化が大きいことが確認された。
この影響は、主要国、新興国を問わず、また、自動車産業、電気・電子機器産業等の製造業を始め、観光関連産業や飲食業等サービス業まで幅広い業種にわたっているが、医薬品産業においては、2020年1~3月期、4~6月期いずれにおいても、そのビジネスが受けた負の影響は他産業に比べて軽微であった。また、COVID-19感染拡大によって国際物流や海外生産拠点の機能が停滞する結果、海外調達製品群の輸入減に伴う国内における医療用医薬品の供給不足や停止が一時懸念されたが、幸なことに大事に至らずに済んだ。これは、かつて新型インフルエンザ感染症パンデミックの国内波及が懸念された際に必要な対応策と認識した、主に代替製品がない、あるいは供給が限定的な医療用医薬品を中心として、その想定必要量の生産、供給を担保するために原薬と最終製品の十分な在庫を製薬各社が確保することに努めてきたことが奏効した結果と言えよう。
医薬品の安定供給:ハードよりソフト面の充実が重要
予断を許さないCOVID-19感染再拡大や新たな感染症パンデミックを踏まえて設置された「医療用医薬品の安定確保策に関する関係者会議」では、海外からの調達依存度の高い医薬品を中心に、国際物流の停滞による供給不足、停止に対するリスクマネジメント策として、在庫量の確保と共に国内生産力の維持策等が論じられ、2020年9月には安定確保医薬品12)を対象とする「供給不安を予防する取組」、「供給不安の兆候をいち早く捕捉し早期対応に繋げるための取組」、「実際に供給不安に陥った際の対応」よりなる取組が取り纏められている。将来、国際物流や海外生産機能の停滞がどの程度の期間継続するかという点がポイントとなるが、今回の経験から、凡そ半年分相当の製品、原薬在庫を確保することで、数カ月間の国際調達製品群の供給回復まで医薬品の供給を十分維持できることを実証したと言え、少なくとも生産拠点の国内回帰のニーズはあまり高くないように見受ける。また、在庫維持に要するコストと国内生産拠点を新・増設、維持するために要するコストとの費用対効果比較も考慮する必要があるが、そのコストと時間を勘案すると、代替製品がない、あるいは供給が限定的な医薬品にのみ焦点を当てた国内生産回帰策が最優先の選択肢とは必ずしも言い難いところである。
新たな感染症パンデミックに既に確立した在庫管理等の対策をより効果的、機動的に運用するためには、ハード面の強化よりも、世界中のコントロール困難な感染症に関する情報の収集と関係機関、業界へのより迅速かつオープンな共有を可能とするソフト面での対策強化が重要であろう。そのためには、製薬協をはじめ、日本経済団体連合会(経団連)、東京都などが提言している、司令塔機能としての役割を果たす専門機関の設置が望まれるところである。そのモデルと言われる米国CDC(Centers for Disease Control and Prevention;疾病対策予防センター)は、疾病、傷害、および障害の防止と管理により、健康と生活の質の向上を使命とした非常に守備範囲の広い役割と機能を有している。ここでは、特に感染症分野に特化し、例えば、CDC傘下のNCIRD(National Center for Immunization and Respiratory Diseases;国立予防接種・呼吸器疾患センター)や、CDCとは別の組織であるNIH(National Institutes of Health;国立衛生研究所)傘下のNIAID(National Institute of Allergy and Infectious Diseases;国立アレルギー・感染症研究所)のような研究機能を併せ持った機能の設置を意図している。
研究開発促進:新興感染症対策に向けたインフラとインセンティブの充実が重要
いうまでもなく感染防止と社会的、経済的活動の活性化を両立するために治療薬やワクチンの開発成功は重要である。前述のように国内でも製薬企業を中心に鋭意注力しているが、現状の開発ステージを比較すると欧米企業の後塵を拝していることは否めない。その要因として、感染拡大初期における情報とその量、それに対する感度に加えて、未知の病原感染因子を取り扱う研究環境などにおけるわずかな差の相乗作用によってもたらされた初動の遅れが考えられる。未知の病原感染因子の研究を進めるにあたり、少なくともその病原性等が明らかとなるまでは有効な治療法がなく特に致死率が高い病原体と同等の高度の封じ込め実験施設(BSL-4(バイオセーフティレベル-4)施設)13)の利用が研究者のリスク低減の点で望ましいが、国内では、1施設が稼働中、1施設が建設中という状況で、10施設以上を保有する米国とは大きな開きがある。また、医薬品候補物質のSARS-Cov-2に対する抗ウイルス効果検証研究等に必要な実験施設(BSL-3)数も限られており、司令塔専門機関への設置と共用促進が即時対応に必要であろう。
ところで、新規医薬品の製品化に必要な研究開発に長期間を要し、その成功確率が非常に低いことは、最近、一般にも徐々に認知されつつあるが、それ故に投資の回収という点でビジネスリスクが高い。わけてもCOVID-19のような流行性新興感染症の場合、更に研究開発リスクは高く、かつ将来の市場性が不透明なため、治療薬やワクチンの製品化加速と十分量の供給確保のために公的な経済支援が重要となる。COVID-19対策として、既に国内外で対応が図られているように、製品化に向けた資金支援、いわゆる"プッシュ型インセンティブ"と、上市された際の価格や政府による買い取り条件についてもあらかじめ保証するといった"プル型インセンティブ"の両輪が機動的に発動される仕組みが平時より確保されていることも、将来の新興感染症パンデミックへの備えとして有効と考える。
ワクチン供給:製造キャパシティの確保が必要
最近の報道によると、日本政府が、海外の製薬企業と、開発成功時のワクチン供給に関する契約を取り交わし、その数量は数千万から1億回投与分という多大な量だという。研究開発が成功し供給を受ける際には、国内で最終製品を製造する品目もあるようで、既にその受託先の目途もついていると聞くが、2017年における国内のワクチン総生産量相当量と見積もられ14)、各国がワクチン確保に動いている中、将来の新興感染症パンデミックに対する備えという観点からも、国内での十分な製造拠点確保も重要な課題になると考えられる。さらに、有効で安全なワクチンが入手可能となり、菅新政権が目指す全ての国民に行き渡る量のワクチンが確保された際には、全国で混乱なく確実にワクチン接種が行われるために、恐らく必要となるであろうコールドチェーンの確保、接種体制の整備が重要であり、行政と医療機関、そして製品供給サイド間の緊密な連携が解決の鍵となろう。
おわりに
今回のCOVID-19パンデミックでは、医薬品産業は、初期対応としてその社会的使命を果たすことができた一方、今後の感染拡大を抑え込むために有効な治療薬、ワクチンの開発、製造、供給に向けて改善、解決すべき課題を再認識することができた。その課題に対する対策は、将来の新興感染症パンデミックへの備えにも繋がるものとなるが、確実に達成するためには、産学官間連携が必要であり、特に司令塔専門機関の設置は、国民の健康維持に直結する戦略として重要なものとなろう。
過去を振り返ると古くは黒死病と言われたペスト、天然痘、インフルエンザ、発疹チフス、エイズ、SARSなど、人類は様々な致死性感染症パンデミックの脅威に曝され、大きな犠牲を払いながらも克服をしてきた。かつては公衆衛生面で劣悪な生活環境下にあったことに加え、原因の特定が困難であったことが大きな犠牲を払う結果に繋がった。COVID-19では、感染拡大から1か月が経ったかどうかという短期間に原因ウイルスが特定され、そのゲノム配列が決定され、1年もたたずに遺伝情報を利用した複数のワクチンが世界中で開発後期段階あることは、喜ぶべき驚きである。これは、ひとえにライフサイエンス関連技術の進歩とデジタル技術に支えられた情報共有のなせる業であり、将来起こり得る新興感染症パンデミックに対しても同様に対応できる可能性が示唆され、未知の新興感染症に対し必要以上に恐怖を感じる必要はないのかもしれない。その一方で、公衆衛生面のインフラが整備されている国々を中心に多数のCOVID-19による死者が発生し、不幸にも全世界で100万人を超えた事実は、どのような教訓を示唆しているのか。
ロックダウンなどによりかつてはあたりまえのように送っていた心地よい日々の生活が奪われた世界中の人々の目や耳に入る膨大な量の情報の中に、信用したい誤った情報も多く含まれているために、それらを理由に、例えば3密回避の対策を取らないなどといった不適切な行動を取ってしまい、クラスター感染や症状の重篤化、その結果として一部では取り返しのつかない転帰に繋がってしまった可能性は一要因として否定できない。いまだにワクチンや有効な治療薬がない中、今後しばらくの間はCOVID-19リスクと共存しながら社会活動、経済活動を進めてゆかなければならないと考えると、感染症拡大抑止にとって最適な行動に繋がる正しい情報提供と正しい理解が必須であり、政府、行政、国民すべての関係者が相互に役割を果たして社会基盤ともいうべき情報リテラシーの向上に向けた努力を続けることが重要である。
斯様に正しい情報をいち早く手にし、適切な対策と必要な行動指針を策定し、更に新たな情報等に基づき最適化をして、タイムリーに国民に伝えること、また、併せて国民が日頃から感染症パンデミックに対する正しい知識を身につけられるような教育あるいは啓発活動が重要であり、そのためにも司令塔専門機関を中心に産学官が連携して機能することが重要と考える。
(本稿は、「産業立地」誌 59巻5号 2020年9月号(一般財団法人 日本立地センター)に寄稿した「医薬品産業のCOVID-19パンデミックへの対応、そして今後に向けて」をもとに、一部改訂を行ったものである。)
-
1)SARS-CoV-2は、人類に重篤な呼吸障害(Severe Acute Respiratory Syndrome)をもたらした2番目のコロナウイルス(CoV:Coronaviruses)の略称であり、COVID-19はcoronavirus disease 2019の略称である。
-
2)新型コロナウイルス感染症に対する国内製薬会社の取り組みは、日本製薬工業協会の特設サイトなどでも公開されている。
-
3)「新型コロナウイルス感染症への対応とその影響等を踏まえた診療報酬上の対応について」、中央社会保険医療協議会 総会(第464回)
-
4)
-
5)
-
6)製薬企業における業務継続のための新型インフルエンザ対策ガイダンスを策定(2008年7月16日)
-
7)
-
8)Samik Upadhaya, et al.,「Impact of COVID-19 on oncology clinical trials」 Nature Reviews Drug Discovery, vol19, p376-7, 18 May 2020.
-
9)BioCenturyに掲載されている情報(2020年8月3日アクセス)より筆者集計
-
10)日本製薬工業協会「製薬協加盟各社による、治療薬・ワクチンの研究開発の取り組みについて」(2020年8月4日アクセス)
-
11)理化学研究所、報道発表資料(2020年8月4日アクセス)
-
12)日本医学会傘下の主たる学会の各専門領域において、医療上必要不可欠であって、汎用され、安定確保が求められる医薬品として提案されたもので、我が国の安全保障上、国民の生命を守るため、切れ目のない医療供給のために必要で、安定確保について特に配慮が必要とされる医薬品を言う。(医療用医薬品の安定確保策に関する関係者会議取りまとめ、令和2年9月;https://www.mhlw.go.jp/content/10807000/000676422.pdf
-
13)国立感染症研究所では、SARS-Cov-2はバイオセーフティレベル3で、また、感染疑いのある患者由来の臨床検体は同2で取り扱うことと定めている。https://www.niid.go.jp/niid/ja/byougen-kanri/9367-n-cov-bio.html
-
14)第35回厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 資料(2019年11月8日開催)

