Topics 新型コロナウイルス感染症(COVID-19)予防・治療薬のグローバル研究開発動向
医薬産業政策研究所 主任研究員 鍵井 英之
1. はじめに
2019年12月31日、中国武漢で発生した原因不明の新型肺炎として報告された新型コロナウイルス(SARS-CoV-2、それによる疾患はCOVID-19と命名された)は、瞬く間に世界中に広まった。WHOのウェブサイト1)によると、6月8日時点の感染者は690万人、死者40万人を超えている。世界各国が法的な拘束力を有するロックダウンを行い、国内においても緊急事態宣言が発令され、人々の移動が制限されるなど経済にも甚大な影響を及ぼしている。行政、医療関係者をはじめとする多くの方々の尽力もあり、欧米各国に比べて国内の影響は少なかったとはいえ、人々の健康、安全、安心を支える医薬品の果たす役割の大きさを改めて認識するものであった。
新型コロナウイルスの症例報告から約半年経った5月末現在、世界各国でワクチンや治療薬の開発が急ピッチで進んでいる。国内でもレムデシビル(ブランド名:ベクルリー)が緊急承認され、アビガンやアクテムラなどの臨床試験も進められている。各国当局もコロナウイルスのワクチン・治療薬開発を科学、規制、審査、資金など様々な方面から支援している。
COVID-19に対するワクチン/治療薬が世界的に待ち望まれる中、本稿では、日米欧各国当局の動きなどに触れると共に、COVID-19関連薬のパイプラインの動向に関して調査を行った。
2. 各国政府・当局の動き、国際協調など
(1)米国
米国では、3月31日に米国食品医薬品局(FDA)がCOVID-19治療薬の開発を加速させるための官民パートナーシップ「Coronavirus Treatment Acceleration Program(CTAP)」を立ち上げた2)。このパートナーシップの下、FDAは研究者や製薬企業に対し、速やかな科学的もしくは規制上の助言を行っている。また、COVID-19治療薬開発に関する臨床試験前相談(pre-IND相談)および臨床試験を実施するにあたって参考となるガイダンスを5月11日付で公表している。米国国立衛生研究所(NIH)は、新型コロナウイルスの分子機構など基礎的な研究からCOVID-19の診断・予防・治療に至るまで、広範なテーマに対して資金提供を行っており、また自らも臨床試験を実施するなどしている。米国政府はNIHに対して約18億ドルのCOVID-19関連追加予算を拠出し、このうち15億ドル以上がNIAID(米国国立アレルギー・感染症研究所)関連予算となっている3)。4月17日にはNIHが主導で世界的な官民パートナーシップ「Accelerating COVID-19 Therapeutic Interventions and Vaccines(ACTIV)」が立ち上がり、COVID-19関連の研究開発を進めるための仕組み作りやプロジェクトの優先順位付けなどを行っている4)。このACTIVには、"官"からFDA、NIH、ASPR(米国保健福祉省・事前準備対応担当次官補局、パンデミック時の緊急オペレーション機能の中枢を担う)、CDC(米国疾病予防センター)、欧州医薬品庁(EMA)の5つの組織が参加、"民"からグローバルメガファーマに加え、EvotecやKSQ Therapeutics、Vir Biotechnologyといったバイオテック企業、国内企業では武田薬品工業が参加している。さらにNIHは4月29日、COVID-19の診断技術を加速させるためのRapid Acceleration of Diagnostics(RADx)を組織し、今年の秋までの実用化を目指している5)。さらに米国保健福祉省に属する米生物医学先端研究開発局(BARDA)6)が、mRNAワクチンを開発している米国Moderna社に約4億3,000万ドル、米Janssen Research & Development社(SARS-CoV-2に対する薬剤スクリーニング)に1億5,000万ドルなど、総額12億ドルを超える研究資金助成を実施している7)。
(2)欧州
欧州医薬品庁(EMA)はCOVID-19の医薬品開発に関する助言およびGMP実地調査費用を1年間無料とした。また、審査期間の短縮により、COVID-19関連品目の開発を加速させるとしている8)。各国の事例として、イギリスでは、国立衛生研究所(NIHR)と英国研究・イノベーション機構が総額2千万ユーロの新型コロナ関連研究の研究公募を行った。フランスでは、国立保健医学研究機構(Inserm)が運営している国内コンソーシアムREACTingが、新型コロナウイルスに関する基礎から疫学研究まで幅広く20件の研究テーマに対して資金提供を行っている9)。
(3)日本
国内においては、レムデシビルが申請(5月4日)から僅か3日後の5月7日に特例承認された(米国では5月1日に緊急使用許可、欧州ではコンパッショネートユースが認められている)。厚生労働省の通知により、新型コロナ関連薬の開発については治験届提出後30日以内での臨床試験の実施が可能であること10)、最優先で審査や調査が実施されること11)、また公的な研究により一定の有効性及び安全性が確認されている場合には、臨床試験等の試験成績を提出しなくても承認される可能性があること12)、などの措置が取られている。AMEDの取り組みとしては、COVID-19などの新興感染症に関する研究開発に対して、2月13日以降、段階的に総額約84億円が投じられている。加えて5月27日に閣議決定された第2次補正予算案では、新型コロナウイルス関連の研究開発に総額609億円が計上された。内容としては、第II相、第III相試験の支援などを含むワクチン開発推進事業に500億円、新作用機序の治療薬の研究開発に50億円などが含まれる13)。
(4)国際協調
国際協調としては、薬事規制当局国際連携組織(ICMRA)が、世界的なCOVID-19パンデミックに対し、医療機器や医薬品開発への規制面でのサポートを行うことを表明している。14)
WHOが中心的な役割を担う国際協調パートナーシップ(ACT Accelerator)15)は、COVID-19に関する診断、予防、治療に関するイノベーションの加速と公平なアクセスを担う。参加団体は、CEPI(感染症流行対策イノベーション連合)、GAVI(ワクチンと予防接種のための世界同盟)、the Global Fund(世界エイズ・結核・マラリア対策基金)、UNITAID(ユニットエイド)など多くの国際組織に加え、産業界からIFPMA(国際製薬団体連合会、日本製薬工業協会も加盟)などが参画している。中でもCEPIは、世界連携でワクチン開発を促進するため、2017年1月ダボス会議において発足した官民連携パートナーシップであるが、6月9日現在、Oxford大のリコンビナントタンパクナノ粒子に関するプロジェクト(最大388億ドル)など9つのテーマに対して研究資金を提供している。16)
以上は各国の取り組みや国際連携の一例であるが、このように、パンデミックのような非常事態においては、各国政府がリーダーシップを発揮し医薬品開発を促進させていることに加え、国際的な協調による治療薬やワクチン開発推進、審査の迅速化、規制や技術に関する情報共有などが積極的に行われている。
3. 開発薬動向
3.1 新型コロナウイルスの感染メカニズムと薬剤標的
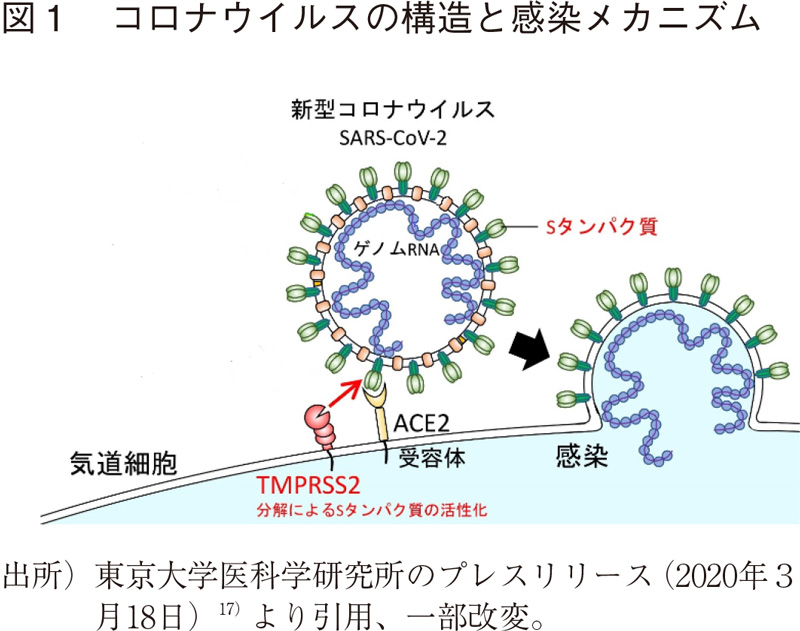
コロナウイルスはRNAウイルスであり、ゲノムRNAとそれを包むエンベロープで構成される。コロナウイルスのエンベロープ表面に存在するSタンパクがヒトの細胞膜上にあるアンジオテンシン変換酵素2(ACE2)を認識、さらに、TMPRSS2という酵素が活性化されることで、エンベロープと細胞膜が融合し、エンベロープ中のゲノムRNAが細胞内に入り込んで、ウイルスの増殖に必要なタンパクやゲノムRNAが合成される(図1参照)。
COVID-19薬剤開発のアプローチとして、ウイルスに対する免疫を誘導するワクチン、Sタンパクなどウイルスの構成タンパクに対する抗体、ACE2およびその関連タンパクの制御、ウイルス関連酵素(RNAポリメラーゼ)阻害、などが挙げられる。レムデシビルやファビピラビル(ブランド名:アビガン)は、RNAポリメラーゼ阻害作用を有する。また、COVID-19では過剰な免疫反応であるサイトカインストームが患者の予後に大きな影響を及ぼすことから、抗IL-6抗体やJAK阻害薬など炎症を抑える薬剤の臨床試験も進められている。
3.2 パイプライン分析
(1)COVID-19開発品目数と開発段階
-
解析対象品目数
本調査では、医薬品データベースEvaluatePharmaを用い、COVID-19の予防(主にワクチン)および治療を適応として開発されている各社のパイプラインデータを抽出し、化合物単位に整理した18)。本調査で分析対象とした品目数を表1に示す。本分析には2020年5月19日時点のデータを用いた。19)

-
開発段階別の品目数
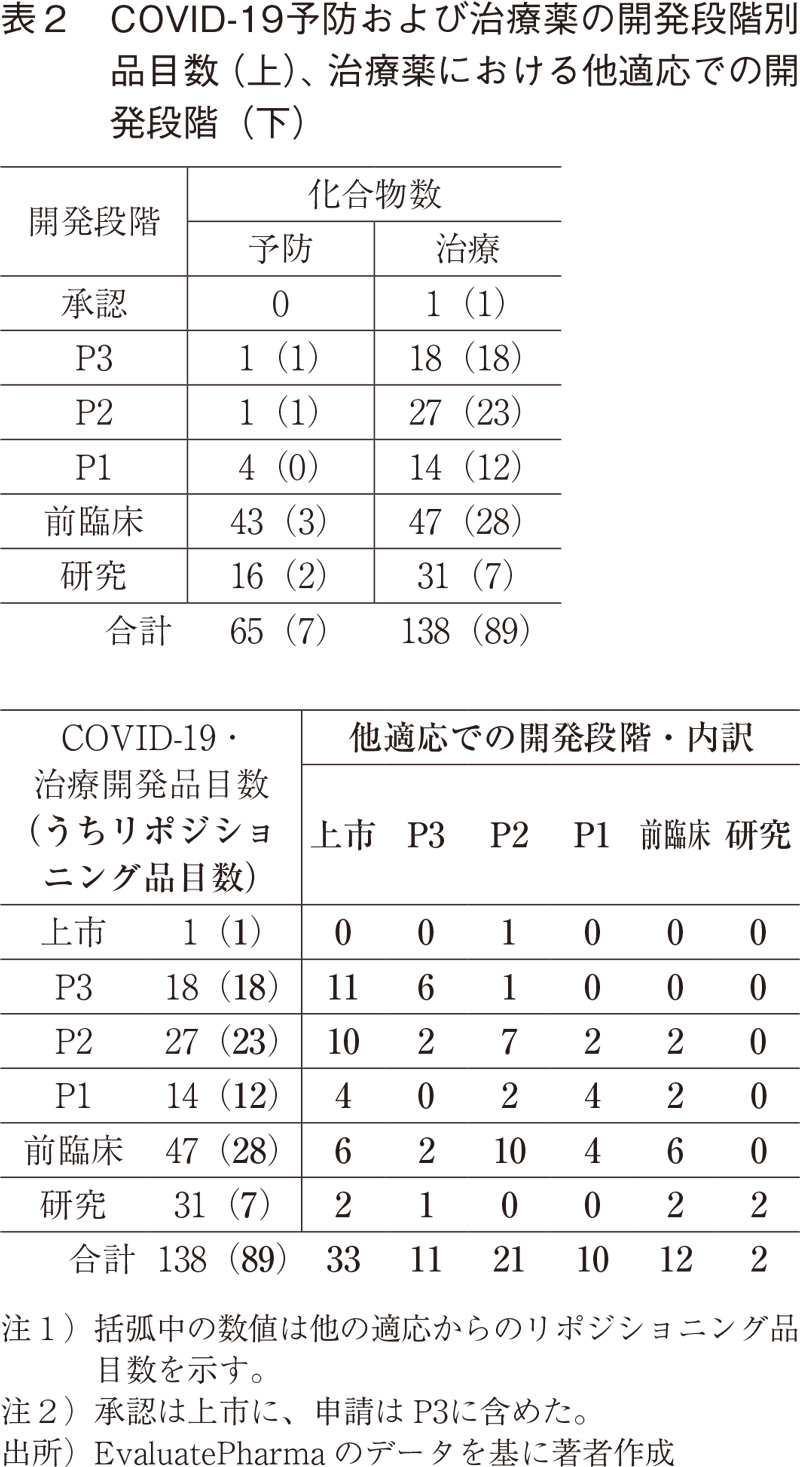
COVID-19関連の開発品について、開発段階別20)の品目数を表2(上)に示す。括弧内の数値は、COVID-19とは別の適応で承認あるいは開発が進められている品目(ここでは、"ドラッグリポジショニング21)品目"と呼ぶ)を示している。予防目的では65品目中7品目、治療目的では138品目中89品目がドラッグリポジショニング品目であった。また、臨床段階に入っている品目では、予防目的では6品目中2品目、治療目的では60品目中54品目がドラッグリポジショニング品目であった。すなわち、治療目的では臨床段階の大半がドラッグリポジショニングであり、早期の治療薬の提供にはドラッグリポジショニングが重要な役割を果たす可能性があることが分かる。
表2(下)では、ドラッグリポジショニング品目について、COVID-19以外の適応(ここでは"他適応"とする)での開発階の内訳を示す。他適応の開発段階は上市(承認含む)が最も多く全体で33品目であるが、第II相(P2:21品目)や前臨床段階(12品目)を含め幅広い開発段階からCOVID-19への展開が確認できた。
(2)COVID-19治療薬に活用されている薬剤
前述の通り、COVID-19治療目的で開発されている138品目中、89品目がドラッグリポジショニング品目であったことから、それら89品目について調査した。表3は、どの疾患領域の薬剤がCOVID-19の治療目的に展開されているのかを示しているが、がん、感染症、免疫領域の薬剤が多い。がん領域からの転用では、キナーゼ阻害薬、TLRアゴニスト、抗PD-1抗体などが確認された。
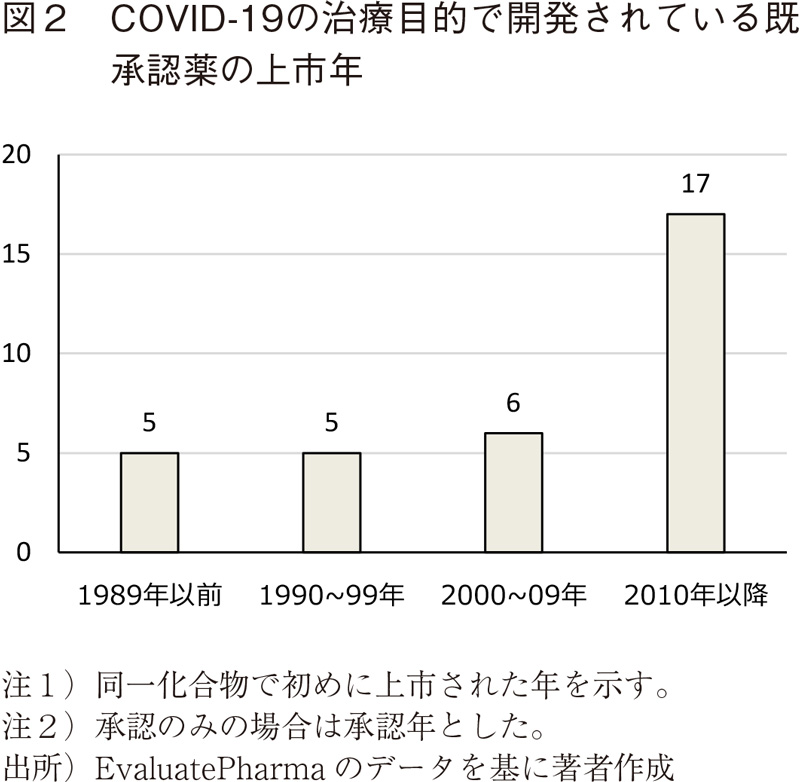
また、89品目のうち33品目が他適応ですでに承認されている薬剤であり、これらの上市年について確認したところ、2010年以降に上市された比較的新しい薬剤が多かった。(図2)

(3)COVID-19開発品(治療目的)の薬効別内訳
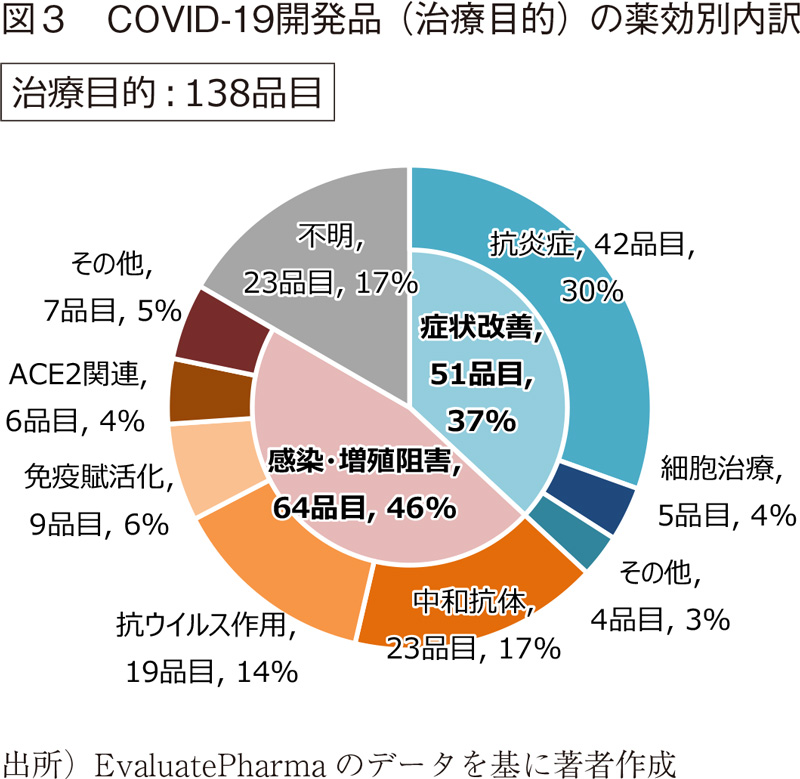
COVID-19治療目的の開発品138品目について、作用メカニズムから分類した薬効別内訳を図3に示す。大きく症状改善(全体の37%)とコロナウイルスの感染・増殖阻害(全体の46%)に分類することができる。症状改善の中心は、サイトカインストームに対する抗炎症作用をターゲットとしたものであり、抗IL-6抗体、IFN-γ調節薬、JAK阻害薬などが含まれる。感染・増殖阻害作用を期待するものとしては、新型コロナウイルスのSタンパクに親和性を有する中和抗体をはじめ、ACE2やRNAポリメラーゼウイルス関連酵素を標的としたものなど、様々な創薬ターゲットでの開発が進められている。
(4)COVID-19開発品のモダリティ分類
-
COVID-19開発品:予防目的
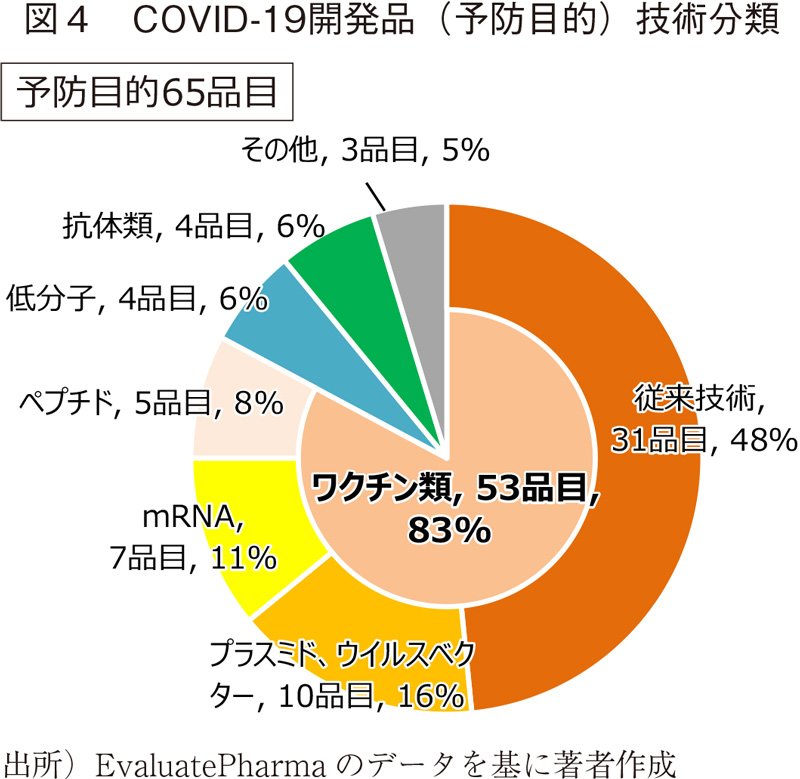
予防目的の開発品65品目のモダリティ分類を図4に示す。ワクチンが全体の80%以上を占める。さらに、ワクチンの技術タイプで細分類すると、不活性化したワクチンもしくは遺伝子組み換えワクチン(現在上市されている主要なワクチンであり、ここでは合わせて"従来技術"と分類している)が最も多くワクチン全体の約6割であるが、残りの約4割はプラスミド/ウイルスベクター、mRNA、ペプチドワクチンなど、比較的新しい技術であった。プラスミド/ウイルスベクターやmRNAを用いたワクチンは、ウイルスタンパクをコードした核酸を投与することで、ヒトの体内で新型コロナウイルスを構成するタンパクが産生され、さらにそれに対する抗体が産生される。ペプチドワクチンはウイルスを構成するタンパクの一部を合成し、それを投与することで、同じく体内で新型コロナウイルスに対する抗体を作らせる。このように、ワクチンの基本的な原理はヒトの体内でウイルスに対する抗体を作ることであるが、様々な技術プラットフォームが活用されている。なお、ワクチン以外の低分子や抗体は、主に治療薬として開発されている化合物の予防的投与であった。
-
COVID-19開発品:治療目的
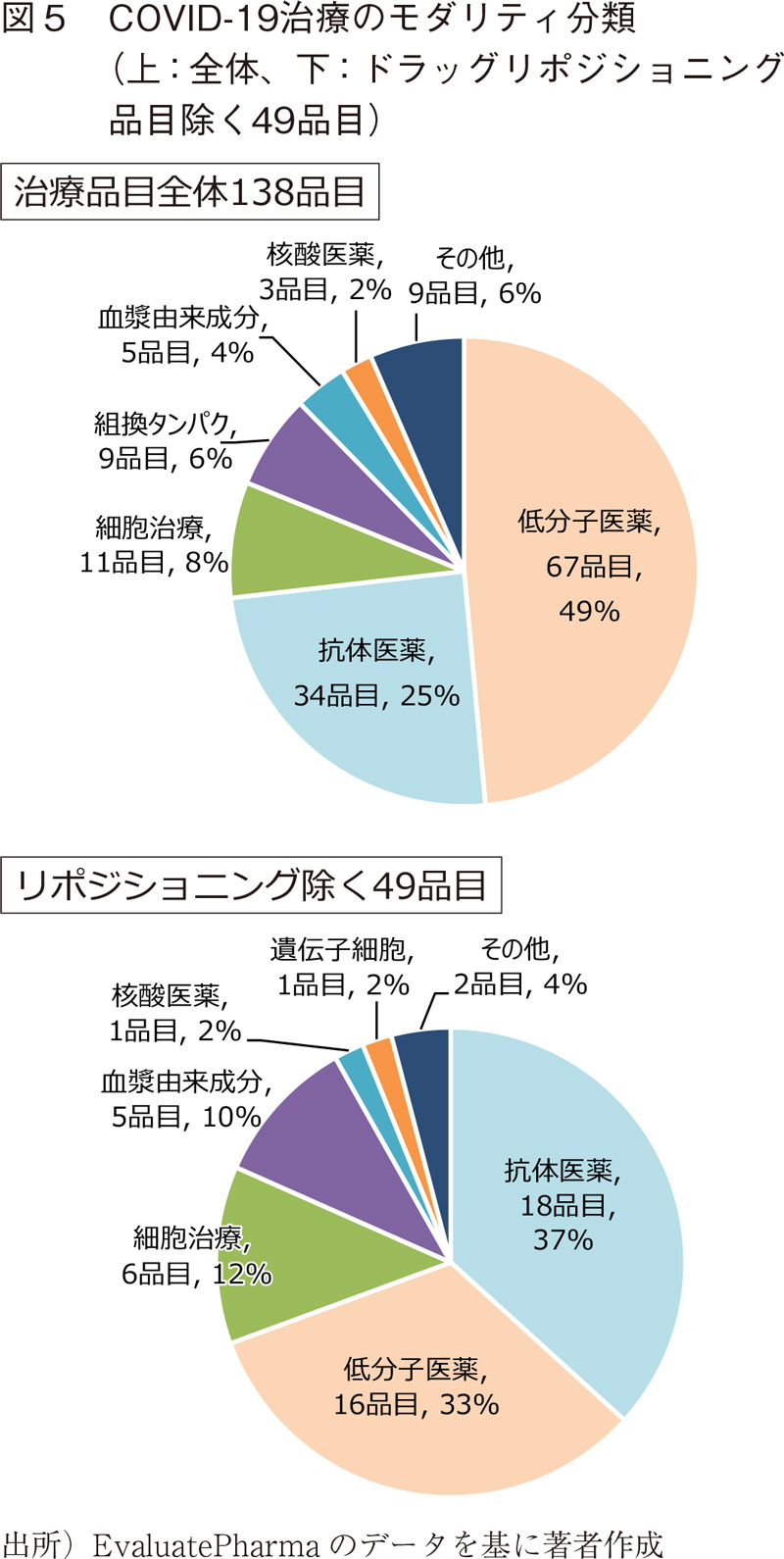
治療目的の開発品のモダリティ分類を図5に示す。全体(138品目、図5上)で見ると、低分子医薬品が約50%であり、抗体医薬品が続いている。前述のように、これらのうち89品目は既存薬からのドラッグリポジショニング品目である。そこで、ドラッグリポジショニング品目を除いた49品目を抽出して同様にモダリティ分類をしたところ、抗体医薬の開発品が最も多く、低分子医薬、細胞治療が続いた(図5、下)。
(5)開発企業の分類と国籍
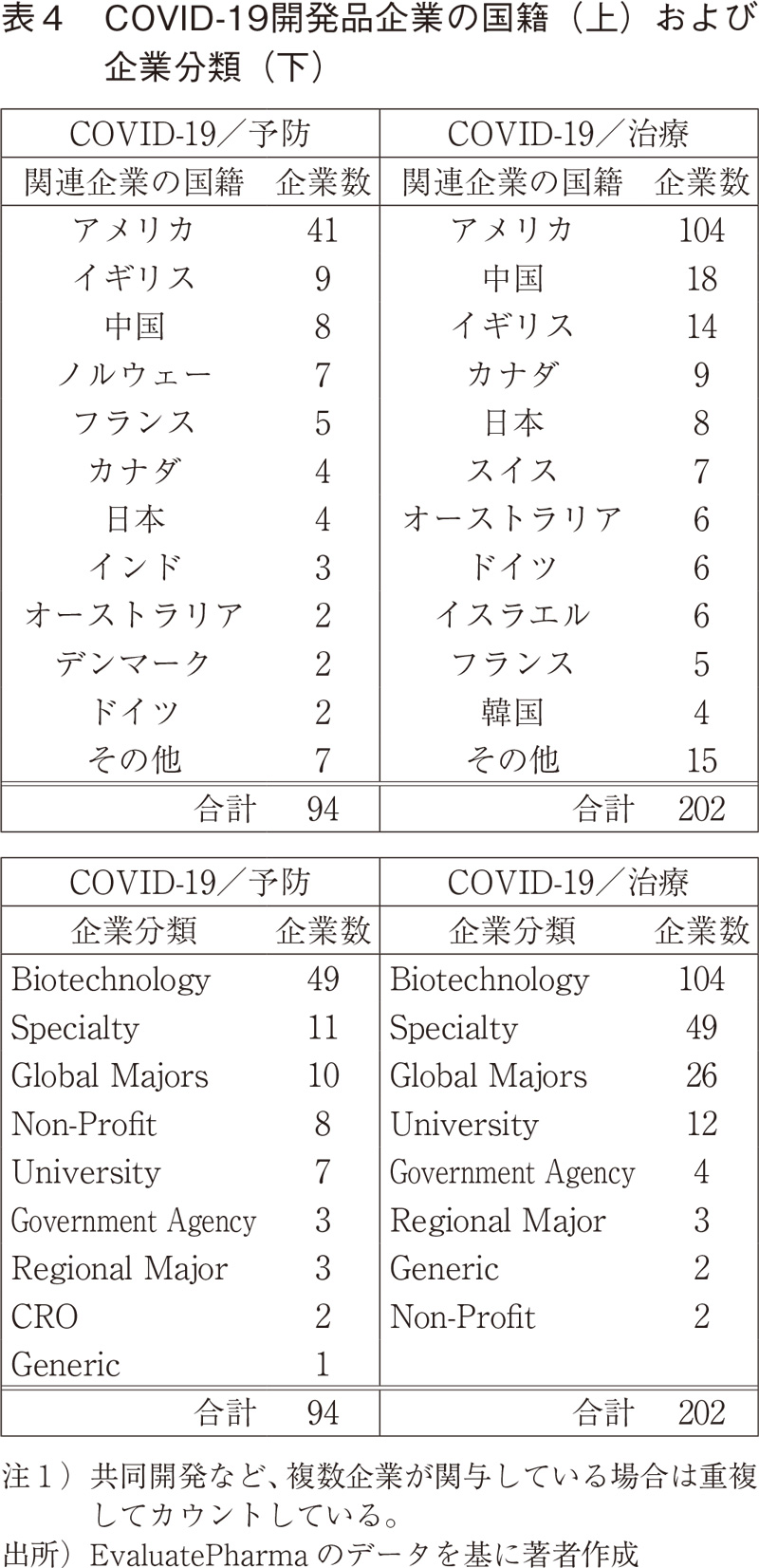
COVID-19予防・治療薬の開発を進めている企業(政府組織や非営利団体も含む)の国籍(表4上)と企業分類(表4下)22)を調査した。国籍については、予防・治療共に米国が圧倒的に多く、中国、イギリスが2~3番目であった。また予防薬では、ノルウェーが7品目確認されたが、これらはすべて先述のCEPI(感染症流行対策イノベーション連合)の関与であった。
企業分類については、予防・治療共にBiotechnology企業が多くを占めたが、大学(University)やCEPIのような非営利組織(Non-Profit)、政府機関(Government Agency)の関与も見られる。
考察とまとめ
本稿では、現在開発が進められているCOVID-19の予防・治療薬に着目し、ドラッグリポジショニングやモダリティ、開発企業の特徴について調査した。COVID-19関連薬の研究開発環境の特徴として、(1)新型コロナウイルスの発生がグローバル規模で研究開発の契機となったこと(世界中でほぼ同時期に研究開発がスタートした)。(2)生命・健康の影響が極めて大きい疾患であること。(3)有効な薬剤が判明していないこと。が挙げられる。本調査は現時点(5/19のデータを用いた)のスナップショットであり、今後も多くの開発品が加わること、また上記の環境が変われば、グローバルの研究開発パイプラインの状況も変化することをまず考慮する必要がある。
新たな疾患にいち早く対応するために、既存薬のドラッグリポジショニングが重要である。COVID-19の治療薬では、多くの既承認薬が活用されており、その疾患領域も様々であった。一方、予防薬(ワクチン)では、ドラッグリポジショニングは少ないが、これはワクチンの特異性が高いという性質上、新型コロナウイルスへの展開が難しいためと思われる(あるいは新型コロナウイルスに既存のワクチンの効果がないからこそ世界中に広がったとも言えるかもしれない)。
ワクチンでは新しいプラットフォーム技術として、mRNAワクチン、ウイルスベクターによるDNAワクチンが注目される。ワクチンに核酸を用いる利点としては、抗原とするタンパクのアミノ酸配列に基づいて塩基配列を自由にデザインできること、核酸自体は生体内に存在する物質であり安全性上の懸念は少ないと考えられること、核酸医薬の開発では血中での安定性が課題の1つであるが、ワクチンの場合は目的のタンパクが発現された後は分解されることが望ましく、一般的に言われている核酸医薬の弱みがワクチン開発の場合は強みとなり得ること、などが考えられる。またmRNAの場合は酵素を用いた人工合成、プラスミドベクターの場合は大腸菌による製造が可能であり、早期に、かつアフォーダブルな価格で提供されることも期待される23)。
COVID-19予防・治療薬の開発は、国籍では米国、企業分類ではバイオテック企業がリードしている。また、CEPIといった非営利団体、政府系機関、アカデミアの貢献が見られることも、今般のパンデミックに対する社会全体の取り組みが表れている。ワクチン開発にスピード感を持って取り組まれている事例として、米国Moderna社のワクチン開発のこれまでの経緯を紹介する24)、25)。
- 1月11日
- 新型ウイルスの全ゲノム情報が公開。
- 1月13日
- NIHと協力してワクチン候補mRNA-1273の配列を確定、製造開始。
- 1月20日
- CEPIに資金援助を求める。
- 1月23日
- CEPIからの資金調達。
- 2月7日
- 臨床第1バッチの製造完了。
- 2月21日
- IND申請。
- 3月16日
- 第I相試験における最初の被験者への投与開始。(臨床試験はNIHが主導)
- 4月16日
- BARDAから最高4億8,300万ドルの資金援助が決定。
- 5月1日
- 世界的な医薬品製造企業であるLonza社と業務提携。
以降Moderna社は、2020年第3四半期の緊急使用、2020年後半の第III相試験開始、2021年の市販化を視野に入れている。
Moderna社がこのような早さで開発を進めることができた要因としては、先述のように、塩基配列でワクチンのデザインが可能である(新型コロナウイルスのゲノム配列の公表後2日後には候補品が完成)という技術的な特徴に加え、スタートアップでは経済的に負担が困難な量産化のプロセスに対して資金提供が行われたこと、規制当局(NIH)の技術的・規制面でのサポートが得られていること、他にもスタートアップならではの機動力(意思決定の速さ)も考えられる。また、世界的な医薬品製造企業であるLonza社と提携したことで、世界的なパンデミックに対応できる製造体制を確保したことも実用化の上では重要である。
国内でも各社が最新の科学を活用してCOVID-19の治療薬・ワクチン開発を進めている26)。製薬企業各社の努力に加え、政府や規制当局、NPOといった社会の後押しを得て新型コロナウイルス制圧に向けた医薬品開発がさらに加速することを願いたい。
-
1)WHOのウェブサイト参照、2020年6月9日アクセス
-
2)FDA、2020年3月31日付プレスリリース参照、2020年6月1日アクセス
-
3)NIH、2020年4月13日付ニュース記事参照、2020年6月1日アクセス
-
4)NIH、2020年4月17日付プレスリリース、2020年6月9日アクセス
-
5)NIH、2020年4月29日付プレスリリース、2020年6月1日アクセス
-
6)化学的、生物学的、放射線、核の脅威や新興・再興感染症から米国を守るために設立された、米保健福祉省の事前準備対応次官補局傘下の組織。ワクチン、医薬品、治療技術、診断技術などの研究開発、FDAによる承認や国家備蓄への移行を、資金的、技術的にサポートする役割を担う。
-
7)日経バイオテク、「BARDA、新型コロナで大小にかかわらず企業に大規模投資」、2020年4月23日
-
8)EMA、2020年5月4日付プレスリリース、2020年6月1日アクセス
-
9)2014年に設立されたフランス研究機関のネットワーク。Inserm本部内に拠点を有し、感染症に関連する疾患研究を調整・支援している。
-
10)厚生労働省、事務連絡、「新型コロナウイルス感染症に係る治験の計画の届出等に関する取扱いについて」(令和2年3月19日)
-
11)厚生労働省、事務連絡、「新型コロナウイルス感染症の発生に伴う当面の医薬品、医療機器、体外診断用医薬品及び再生医療等製品の承認審査に関する取扱いについて」(令和2年4月13日)
-
12)厚生労働省、薬生薬審発 0512 第4号、薬生機審発 0512 第1号、「新型コロナウイルス感染症に係る治験の計画の届出等に関する取扱いについて」(令和2年5月12日)
-
13)日経バイオテク、「日本政府が第2次補正予算で新型コロナワクチンなどに609億円を配分」、2020年6月1日
-
14)ICMRAのウェブサイト、2020年6月1日アクセス
-
15)WHO、2020年4月24日付プレスリリース、2020年6月1日アクセス
-
16)CEPIのウェブサイト、2020年6月8日アクセス
-
17)
-
18)一般名などを基に、同一の化合物を複数の企業が開発していることが確認できる場合は、1品目(1化合物)として扱った。
-
19)開発品の情報は随時アップデートされていることに留意されたい。最新の研究開発情報はWHOやBioCenturyのウェブサイトなどを参考にすることができる。
-
20)グローバルで最も進んだ開発段階を指す。
-
21)本稿では、既承認薬に加え、開発段階からの転用もドラッグリポジショニングとして扱う。
-
22)2020年5月現在、EvaluatePharmaでの製薬企業の分類は、Global Major(世界的大手製薬企業)、Regional Major(新規医薬品を特定の地域で開発、販売する企業。自社で研究開発を行うとともに他の企業や研究機関から化合物、製品のライセンスイン等も行っている。複数の疾患領域をターゲット領域とする。Biotechnology(新有効成分含有医薬品やバイオ医薬品を開発しており、小企業が多く含まれるが、Gilead Sciences、Celgene、Biogenなどの企業も含まれる)、Specialty(独自の研究を行っているが新規医薬品に焦点を絞っていない企業や、一つの疾患領域のみ焦点を当てている企業。)などがある。今回の分析ではBiotechnologyのうち、Global MajorあるいはRegional Majorにも該当する企業についてはそれぞれGlobal MajorあるいはRegional Majorとして分類した。なお、日本の大手製薬企業では武田薬品工業がGlobal Major、他はRegional Majorに分類される。
-
23)日経バイオテク、「パンデミックの救世主となるか、mRNAワクチン」、2020年3月10日
-
24)
-
25)Moderna社プレスリリース、2020年6月1日アクセス
-
26)日本製薬工業協会 ウェブサイト、2020年6月1日アクセス

