Points of View 医療健康分野における医療技術評価の活用のあり方 費用対効果評価の制度化を踏まえて
医薬産業政策研究所 主任研究員 中野陽介
1. はじめに
2019年4月より本邦において、費用対効果評価の制度が本格的に開始した。これは、医薬品、医療機器及び再生医療等製品が対象であり、これまでは主に臨床的有効性および安全性の観点や医療上の有用性から医薬品等の価値は評価されてきたが、そこに新たに費用対効果の観点も取り入れられた。
また最近では、持続可能な社会保障制度の議論がある一方、免疫チェックポイント阻害薬やCAR-T細胞療法などの革新的かつ高額な医薬品の上市によって、特に医薬品の価格や費用対効果に対して世間の関心も集まりつつある。そこで、本邦における費用対効果評価について、制度内容をもとに現状を整理しつつ、医薬品ひいては医療健康分野での費用対効果を含めた医療技術評価(Health Technology Assessment、以後HTA)の今後の活用のあり方について考えてみたい。
2. 費用対効果評価制度の概要
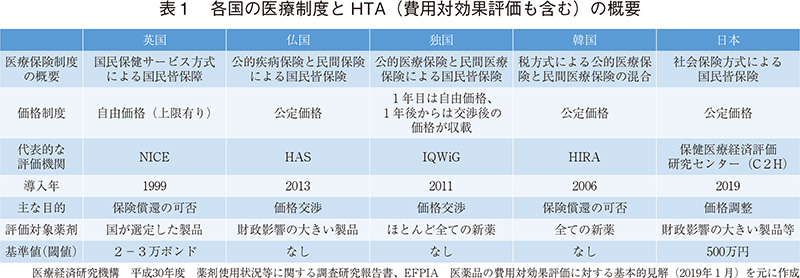
本邦での費用対効果評価制度は、薬価制度の課題として、中央社会保険医療協議会(以下、中医協)において2012年頃から導入の検討が始まり、2016年4月からの試行的導入を経て、本年4月に正式に制度化された。1)諸外国の制度を参照しつつ、本邦特有の薬価制度との整合性および医薬品等への患者アクセスを阻害しないことなどを配慮した上で、制度設計の検討がなされた。諸外国と比較した場合、本邦の制度の特徴は評価結果を公定価格である薬価基準の価格調整に用いる点といえる(表1)2)。本制度の詳細は他稿を参考していだたくとして、ここでは本邦における費用対効果評価の現状を今夏に開催された国内学会等での議論を踏まえつつ、要点を絞って整理する。なお、本制度に対する製薬産業(製薬協)の見解は「費用対効果評価の制度化について」3)の中で表明している。
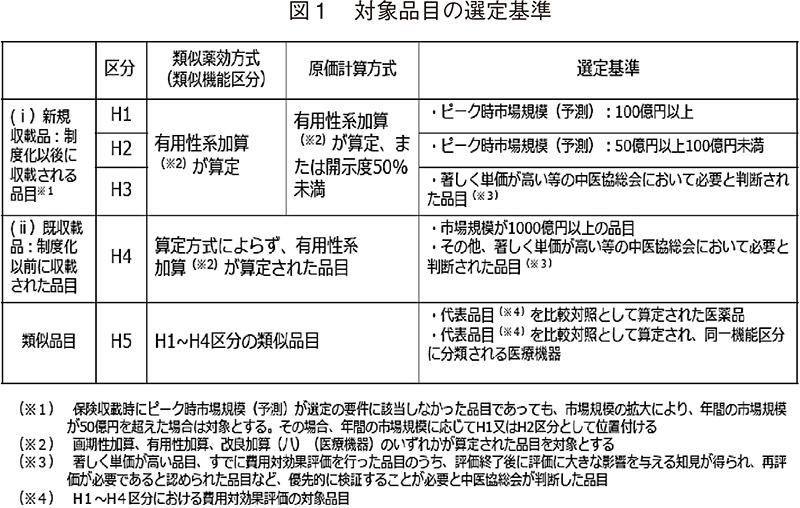
2-1. 対象品目の選定基準
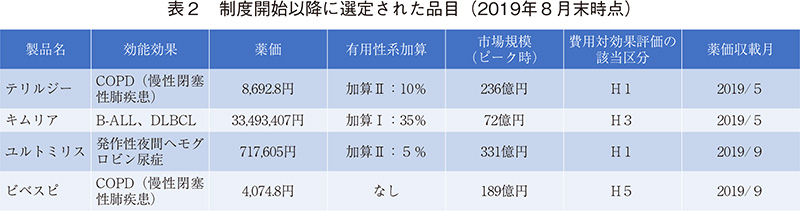
品目の選定基準を図14)に示した。端的に言えば、革新性が高く、財政影響が大きい医薬品が本制度の主な対象となっており、薬価算定方式や選定基準等に応じてH1~H5の5つの区分に分類される。現時点での年間の評価可能品目数の上限は10品目程度と言われているが、公的組織の人的リソースの拡大や経験が積まれていくと、対象品目数が拡大することも想定される。なお、2019年8月末時点までに選定されたのは4品目である(表2)5)。1患者当たりの薬価が約3,300万円となったキムリアについては、予想される市場規模はピーク時年間70億円程度であるが、中医協において著しく単価が高いと判断され、H3として選定されている。
2-2. 評価手法
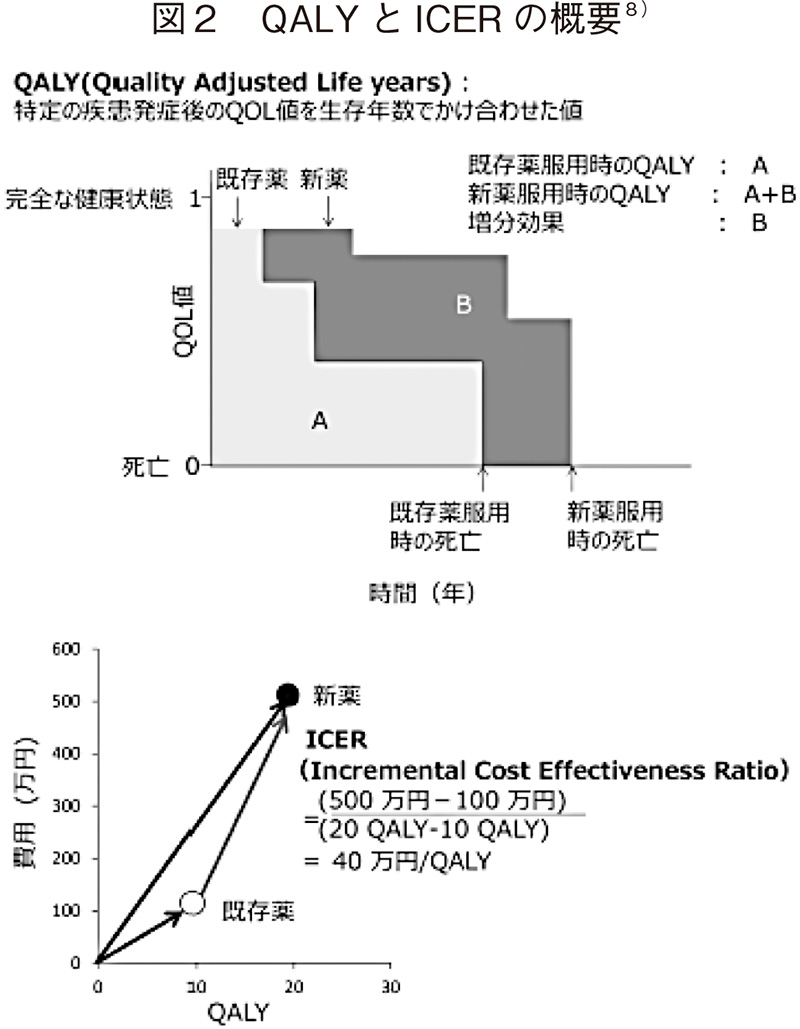
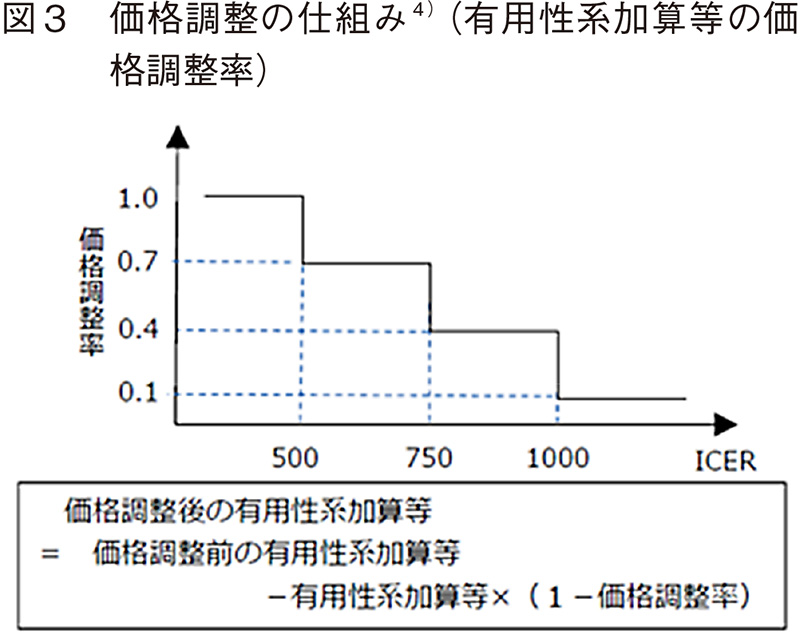
費用対効果評価では、効果指標に原則QALY(Quality-adjusted Life Year:質調整生存年)を用いて、1QALY獲得あたりの費用増分であるICER(Incremental cost-effectiveness ratio:増分費用効果比)で評価する(図2)。この指標を用いることは先行する諸外国と同様であるが、基準値の取り扱いは異なる。本制度では、500万円/QALY(上限、1000万円/QALY)6)が基準値として設定され、算出したICERの値がこの基準値を超えた場合には値に応じて加算部分の価格を段階的に引き下げる調整が行われる7)(図3)。この基準値の妥当性に関しては、支払意思額調査(Willingness to pay)、1人当たりGDPを参照するなど算出方法は様々検討されてはいるが、十分な根拠を説明できるものではなく、専門家の間でも賛否がある。さらに、遺伝子・細胞治療薬のように高額な製品総原価が見込まれる革新的な治療薬が今後も増えていく可能性を考慮すると、この基準値や取り扱いの妥当性等に関する議論は継続していく可能性がある。
2-3. 評価体制・プロセス
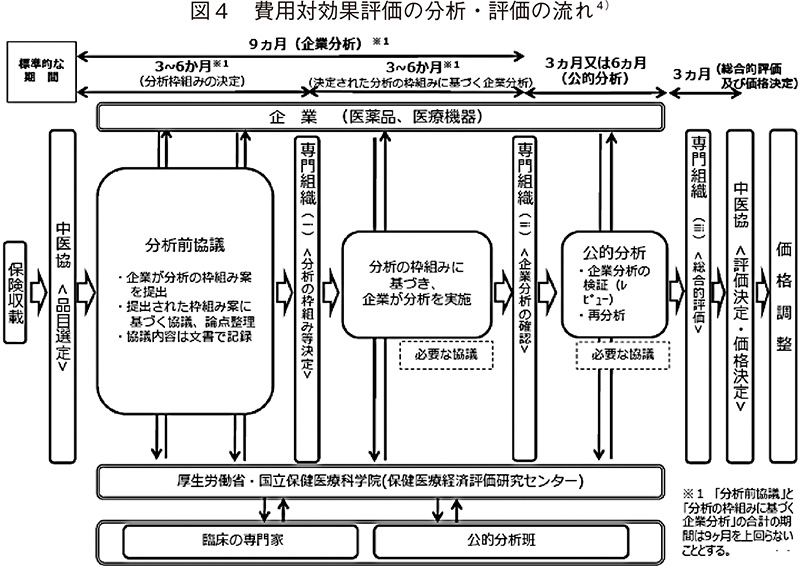
対象品目として選定されると、速やかに分析・評価が開始され、総合的評価の際に、ICER以外の観点も考慮した包括的な判断が下される9)。そして、最終的な評価・価格決定が下るまでには1年から1年半程度を要する(図4)。また、公的な専門組織として、国立保健医療科学院に保健医療経済評価研究センター(通称:C2H)と呼ばれる組織が2018年4月に設置された。2019年9月現在このセンターは6名のメンバーで構成されている。制度的な評価の反映方法を諸外国と比較すると、本制度における総合的評価では、ICER以外の要素を十分に反映する仕組みにはなっているとは言い難い。なお、英国では評価の過程で、患者を巻き込み、患者の声を反映するような仕組みが取り入れられている。10)さらに国際学会International Society for Pharmacoeconomics and Outcomes Research(ISPOR)等でも、医療技術評価のプロセスに患者視点をどのように組み込むべきかといった議論が行われており11)、本邦においても評価プロセスの中に、患者視点の取り入れを望む声はあるため、今後検討が進んでいくことを期待したい。加えて、今後、制度上の課題や修正について製薬産業とアカデミアや学会が協同し検討する場を作り、改善策等を提言するような取り組みも必要ではないかと考えられる。
3. 今後の医療技術評価(HTA)の活用のあり方
以上が本邦の医薬品等に対する費用対効果評価の制度概要であり、医薬品等の"薬価の価格調整"に焦点を当てたものとなっている。しかし、本来、費用対効果の分析は対象を医薬品等のみに限定するものではない。そもそも費用対効果は、HTAを検討する際の有力な観点の一つであり、限られた医療資源をより効率的に配分するための意思決定手法の一つともいえる。12)、13そこで、ここからは医療資源の効率的な配分という視点から、医薬品ひいては医療健康分野における費用対効果を含めたHTAの今後の活用のあり方や課題について考えてみたい。なお、その視点から見た場合に、HTAに求められる重要な要素は、「価値の適切な評価」と「医療の効率化の判断」であると考えられ、その観点から考察を行った。
3-1. 価値の適切な評価
多面的な価値の評価
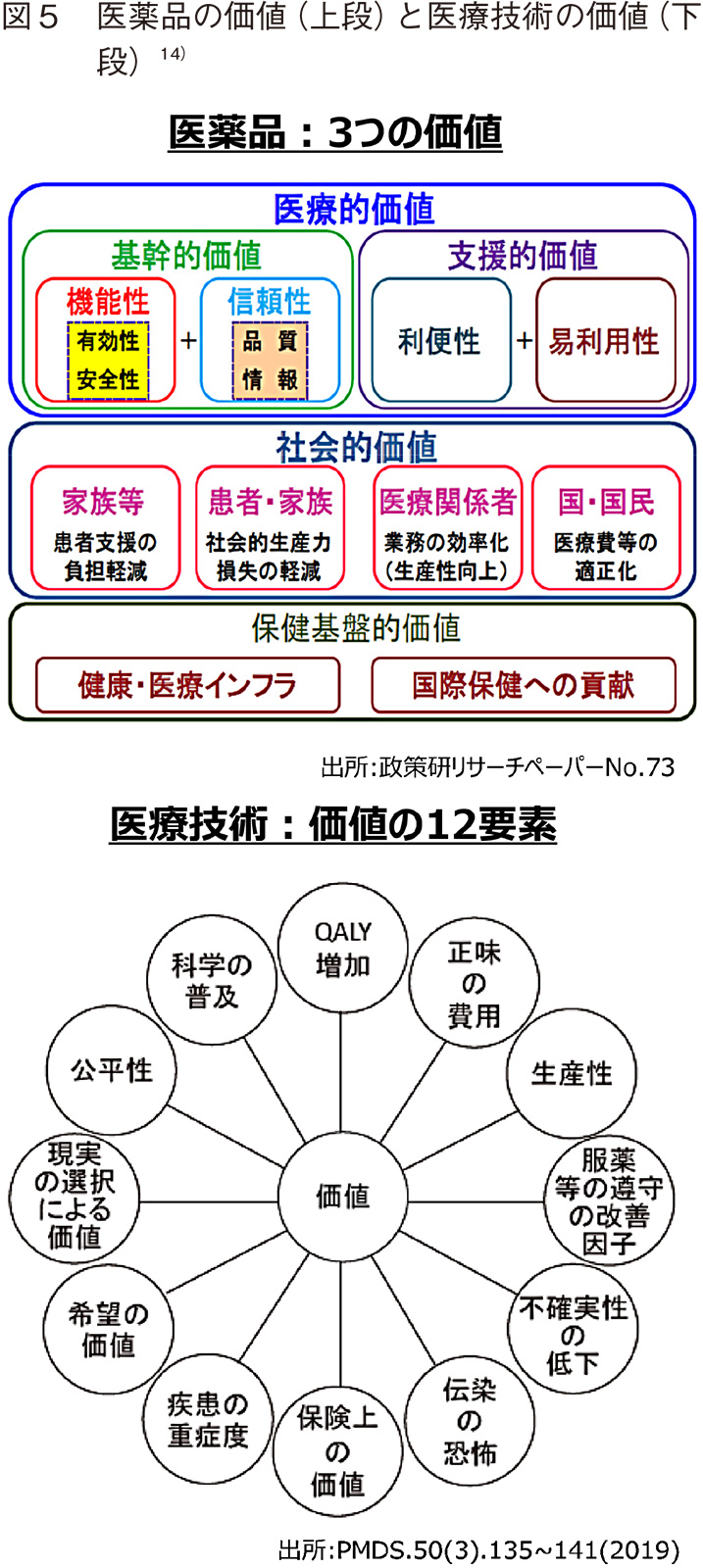
超高齢社会に直面する本邦において、医療健康は個人だけでなく社会全体での課題である。社会課題の解決には、行政や産業だけでなく市民や患者の協力も必要不可欠であり、さらには課題に対するソリューションが個人に加え、社会にとってどのような価値をもたらしたのかといった視点や評価も当然重要となってくる。医薬品や医療技術においても例外ではなく、これらがもたらす多面的な価値をいかに評価し、HTAに取り込んでいくのかといった検討が求められる。一例として、これまでに検討されてきた医薬品および医療技術に関する価値の要素を図5に示すが、その要素は医療経済性の視点にとどまらない。そのため、前述したICER(QALYと費用)という評価だけで医薬品や医療技術の価値を評価するには限界があると言える。その価値としては、患者自身にとっての価値や医療的な価値を超えた社会的な価値も重要であると考えるが、「患者自身の価値」や「社会的な価値」の立場から医薬品や医療技術を評価するのは容易ではない。なぜならば、それらの価値の要素をどのようなアウトカム指標として定めるか。そして、そのアウトカムをどうやって測定するのかといった基本的な課題が解決されていないからである。他方で、最近では患者自身の評価(Patient Reported Outcome)の取得や活用検討が活性化しており、さらにはデジタル技術の進展により、これまでは取得もしくは活用が難しいと考えられていたような患者データ(声、動作、感情など)もデジタルデバイスやセンサー等を駆使することで、データ取得が可能な状況になりつつある。また、個々人の医療・健康・介護のデータを長期的に収集・連結できるような環境整備も国が中心となって進めている。以上のことから、将来的には新たなアウトカム指標や測定が可能になり、医薬品等の多面的な価値の評価が進展していくことが期待される。そのような進展を見据え、IoTやセンサー、デジタルといった測定技術革新とデータの顕在化も注視しておく必要がある。
イノベーションへの対応
いま医療健康分野では著しいイノベーションが起こり始めている。ゲノムデータ等に基づく個別化医療、医療健康に関する様々なデータを活用したソリューションの開発、デジタルセラピューティクスや遺伝子治療等の新規モダリティの開発・上市など新しい動きがある。このような従来の概念では評価が難しい革新的な治療や医療技術をどのように評価していくかはこれからの大きな課題である。遺伝子変異に基づく臓器横断的な適応を持つ抗がん剤の評価を例にとると、臓器別の適応症ごとに評価を考えていくという方法では価値を十分に評価できていない可能性がある。また、がんゲノム医療が普及していく過程では、検査および治療を含めたがんゲノム医療のソリューションとしての価値評価に注目が集まることも想定される。
さらに海外に目を向けると、例えば、英国NICEは前述のような医療環境の変化を踏まえて、技術評価(TA)や高度先進技術(HST)などの評価手法の見直しを行うことを発表した。15)また、米国の非政府HTA組織である「ICER」でも遺伝子・細胞治療薬等(Single or Short-Term Transformative Therapies:SSTs)の登場を踏まえ、その特性に見合った価値の評価方法の検討が始まっている。16)
これらの先端医療や医薬品の価値評価では現在の評価指標が必ずしも適切ではないものもあり、評価の期間もこれまで以上に長期の視点が必要な評価もある。このような評価に際しては新たな評価手法の開発なども必要になる。
3-2. 医療の効率化の判断
保険償還等の判断
社会保障費の増大抑制が喫緊の課題である本邦において、費用対効果を医薬品や医療機器の保険償還の可否や償還率を判断する手段として利用すべきとの主張がなされることも考えられる。実際に表1で示したように、英国や韓国等ではHTAの結果が保険償還の判断にも使用されており、専門家の中にもそのような活用を推す者もいる。本年9月より政府は全世代型社会保障検討会議を開催しており、この中でも同様の主張がなされ得ると見込む。医療の効率化の視点で考えると、同じ効果を上げるために最も費用や労力が少なくて済む医療介入はどれなのか、あるいは、便益を最大にする医療介入はどれなのかといったアプローチは重要であり、新たな医療技術やサービスの導入にもそのような評価・判断は必要かもしれない。しかしながら、皆保険制度の持続を目指す本邦においては、保険償還の可否判断は医薬品や医療機器等の患者アクセスを阻害することも懸念されるため、慎重な議論が望まれる。
医療健康分野全体への普及
本邦における費用対効果の活用は、医薬品等に偏っており、一般の診断治療や医療プロセスといった医療技術に係るところでは、活用が限られている。これから疾病予防や健康維持への介入の重要性が増していく中で17)、予防接種以外の疾病予防においてもHTAに基づく意思決定が広がっていくことが期待される。一般に疾病予防において、医療費削減の効果を実証するのは難しいと言われているが、デジタル技術を活用した低コストの介入方法などによって、費用対効果等にも優れる疾病予防策の研究が進んでいくことが望まれており、その費用対効果を証明していく必要性も高まっていくことが想定される。
さらに、医療(診断・治療・リハビリ等)技術の評価においても、費用対効果の概念が少しずつ広がりつつある領域もある。例えば「心血管疾患におけるリハビリテーションに関するガイドライン」には費用対効果の考え方が取り入れられており18)、他の一部の診療ガイドラインでも導入に向けた動きがあると言われている。本邦の医療やヘルスケア全体の効率化や費用負担のことを考えると、将来的にはこの費用対効果ひいてはHTAという視点が診療報酬を含めた医療健康分野で横断的に広がっていくことが必要であろう。
4. まとめ
以上、本邦で制度化された費用対効果評価についての現状を踏まえつつ、医薬品ひいては医療健康分野での今後の費用対効果を含めたHTAの活用のあり方等について検討した。現在、医薬品等に対する本邦の費用対効果の役割は、"薬価の価格調整"に限定されている。しかし、Precision Medicine/Healthcareに向かって、医療の概念が治療から予防・健康維持へと広がっていく中で、単に現在の治療の範囲で費用対効果を検討するのではなく、ヘルスケア全般にわたって、更には社会的な立場等に立った検討の必要性が生まれつつある。
また、進展するデジタルやIoT、AI等の革新的な技術を積極的に活用し、評価指標や手法が拡大されていくことも期待したい。費用対効果評価ひいてはHTAに資する研究を担う人材が産官学ともにまだ少ないという課題はあるが、医療健康分野において限られた医療資源をいかに効率的に投入していくかという意思決定のための研究は極めて重要である。
木を見て森を見ずの議論にならぬよう、本邦にとって費用対効果を含めたHTAの取り組みが医療健康分野全般に普及・発展していくことが望まれる。
-
1)中医協 費用対効果評価専門部会 費用対効果評価の試行的導入について(概要)(平成28年4月27日)
-
2)医療経済研究機構 平成30年度 薬剤使用状況等に関する調査研究報告書、EFPIA 医薬品の費用対効果評価に対する基本的見解(2019年1月)を元に著者作成
-
3)
-
4)中医協 費用対効果評価専門部会・薬価専門部会・保険医療材料専門部会合同部会 資料(2019.3.27)
-
5)中医協 総-1-1 元.5.15、中医協 総-1-1 元.8.28 資料を元に著者作成
-
6)抗がん剤等の場合:750万円/QALY(上限:1500万円/QALY)
-
7)評価結果がICER200万円/QALY未満orドミナント等で、さらに一定の条件を満たした場合、価格の引き上げを行う仕組みがある
-
8)医薬産業政策研究所、政策研ニュースNo.52(2017年11月)
-
9)総合的評価では分析結果の妥当性を科学的な観点等から検証するとともに、倫理的な観点なども含めた評価が行われる。また、総合的評価によって配慮が必要な品目(希少疾患、小児疾患、抗がん剤等)が選定される。
-
10)桜井なおみ、患者目線からみた費用対効果評価 薬剤疫学 23(1) Jan 2018
-
11)ISPOR 日本部会ニュースレターNo.8
-
12)CRDS、医療の持続的発展に向けた戦略的な医療技術評価(Health Technology Assessment)の推進、CRDS-FY2011-RR-08
-
13)白岩健、保健医療における費用対効果の評価方法の概要とデータの整備について、保健医療科学 2017 Vol.66
-
14)医薬産業政策研究所、「「医薬品の価値」をあらためて考える」、リサーチペーパー・シリーズNo.73(2019年5月)、鎌江伊三夫 第7回 続・医薬経済学から見た価値と価格の関係、PMDRS、50(3)、135~141(2019)
-
15)NICE announces details of health technology evaluation methods review(2019.7.22)
-
16)ICER Value Assessment Methods for "Single or Short-Term Transformative Therapies" (SSTs)NICE announces details of health technology evaluation methods review(2019.8.6)
-
17)
-
18)心血管疾患におけるリハビリテーションに関するガイドライン(2012年改訂版)

