Points of View
医薬品開発におけるウェアラブルデバイスの活用状況
-2025年6月までの動向分析-
医薬産業政策研究所 主任研究員 富樫満里子
医薬産業政策研究所 主任研究員 渡邉奈都子
医薬産業政策研究所 主任研究員 枝廣誠
要約
- ClinicalTrials.govを用いて、2025年6月末時点の医薬品の臨床試験におけるウェアラブルデバイスの活用状況を調査した。
- ウェアラブルデバイスを用いた試験は2016年に初めて確認され、2019年に大幅な増加が認められた後、継続的に活用されている。また、2025年においては限定的な期間の集計値であるが、登録された試験数に更なる増加の傾向が認められた。
- 実施PhaseはPhase2、Phase4が多く、Phase3では限定的であった。
- 臨床試験の地域別の実施数は、アメリカ合衆国が突出して多く、ヨーロッパ、東アジア等全21か国の登録が認められた一方で、日本の事例は2021年7月に発行した政策研ニュースNo.631)で報告された1件のみであった。
- ウェアラブルデバイスが活用されていた疾患領域は神経系の疾患、精神および行動の障害、循環器系の疾患等であった。また、測定項目としては、睡眠、身体活動、歩行、バイタルをはじめ、多岐にわたる項目が確認された。
- 近年、ウェアラブルデバイスの測定範囲は拡大し、夜間の掻破動作や咳嗽頻度、運動緩慢・不随意運動・振戦などといった運動指標を含む多様な生体情報を、連続的かつリアルタイムで取得可能となった。
1. はじめに
近年、ウェアラブルデバイスは医療・ヘルスケア領域で急速に存在感を高めており、医薬品開発の現場でもその活用が広がりつつある。とりわけ臨床試験では、日常生活下で得られる多様な生体情報を連続的かつ客観的に取得できる手段として注目されており、従来の診察や自己報告では把握が困難であった指標を補完する技術として期待が高まっている。こうした特性は、研究の精度向上や新たな評価手法の構築に資するものとして、本格的な導入が進められている。医薬産業政策研究所では、政策研ニュースNo.63において、医薬品開発におけるウェアラブルデバイスの臨床試験での活用状況を初めて調査・報告した。本稿は、その後の技術的進展や臨床現場での実装事例の蓄積を踏まえ、2025年6月末時点の状況を整理するものである。
ウェアラブルデバイスの性能向上に伴い、その臨床試験における役割は拡大し、活用の目的や方法も多様化している。これまでにない形での評価やデータ収集の可能性が広がる一方、活用に際しては依然としていくつかの課題も残されている。こうした背景を踏まえ、最新の調査結果と具体的な活用事例を示しつつ、利活用の進展とその意義を明らかにし、今後の展望を概観する。
2. 臨床試験におけるウェアラブルデバイスの活用状況
政策研ニュースNo.63と同様の方法を用いて、医薬品の臨床試験でウェアラブルデバイスがどのくらい活用されているのかを調査した。本調査では、2025年6月末時点でClinicalTrials.govに登録されている全試験の中から、以下の条件に基づいて抽出を行った。
- 語句検索:Wearable
- Interventions:Drug or Biological(Device検証試験を除く)
- Study Type:Interventional
この条件に基づき、ウェアラブルデバイスで取得されるデータを活用している試験を選定し、さらに「Start Date」が2025年末までの試験を分析対象とした結果、118件が該当した。
ClinicalTrials.govは、米国国立衛生研究所(NIH)等が管理する臨床試験登録・結果データベースである。米国内で実施される臨床試験は登録が義務づけられており、他国の試験や製薬企業による登録は任意であるが、200か国以上から登録されており、世界最大級の臨床試験データベースの一つとされる。
なお、本調査は「Wearable」の語句検索に基づいているため、ウェアラブルデバイスを活用していても語句を含まない試験は抽出されず、全体件数は限定されている可能性がある。
2-1 調査結果「年次ごとの試験実施件数」
本節の集計では、抽出した118件の臨床試験について、各試験の開始年「Start Date」として記載されている年次ごとの件数をカウントした(図1)。
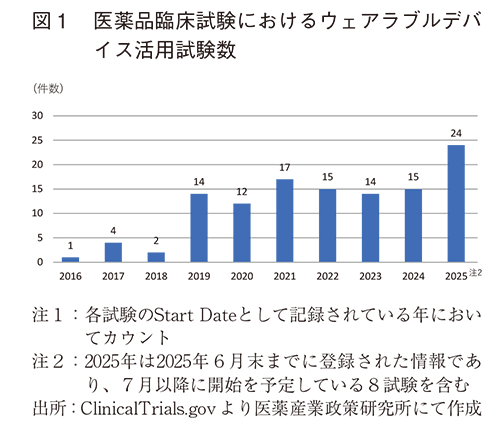
前回の政策研ニュースNo.63で示したように、ウェアラブルデバイスを用いた試験は2016年に初めて検出された。2019年には試験数の大幅な増加が認められ、それ以降は継続的に活用されていることが確認できる。また、2025年においては6月末時点までの限定的な期間であるものの、登録された試験数に更なる増加の傾向が認められるため、引き続き活用の動向を注視する必要がある。
2-2 調査結果「実施Phase」
図2では、医薬品の臨床試験のどのPhaseでウェアラブルデバイスが使用されているかを示した。
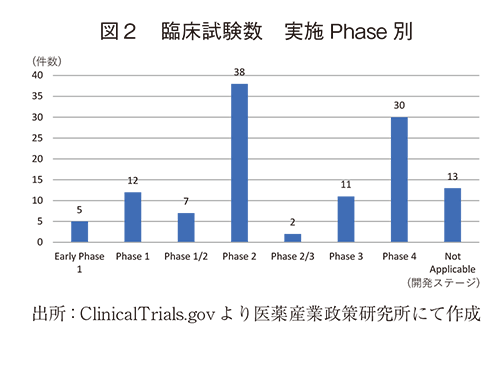
最も多く使用されていたのはPhase2の38件(前回報告12件から増加)で、ウェアラブルデバイス活用試験全体の36%(Not Applicable:13件を除いた105試験中)を占めており、臨床試験全体におけるPhase2の割合(30%)と比べても高かった。次いでPhase4が30件(前回報告14件から増加)で、ウェアラブルデバイス活用試験全体の29%を占め、臨床試験全体の割合(22%)を上回っていた。一方、医薬品の申請の要となるPhase3では、前回報告から件数の増加は認められたものの(6件→11件)、ウェアラブルデバイス活用試験全体の10%であり、臨床試験全体における割合(17%)に比べて低く、限定的であった。
2-3 調査結果「実施主体」
図3では臨床試験の実施主体別に実施件数を示した。
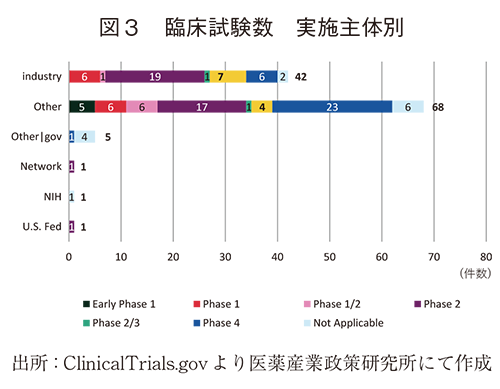
最も多いのはOtherの68件であり、次いでIndustry、Other/govの順であった。Otherには病院、大学が含まれており、前回報告と同様に自主研究などにウェアラブルデバイスを積極的に活用していると考えられた。Other(主に病院、大学)での活用Phaseの傾向は前回報告と比較し、Phase2及びPhase4での活用が増加(それぞれ3件→17件、3件→23件)した。Industryでの主な活用においてはPhase2が最も多く、前回報告からの増加が大きかった(7件→19件)が、その他Phaseにおける顕著な伸びは認められなかった。
2-4 調査結果「実施国」
図4では臨床試験の地域別の実施数を示した。
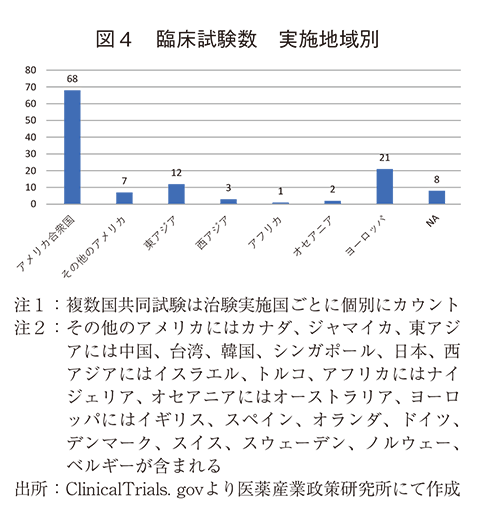
アメリカ合衆国が68件で最も多く、次いでヨーロッパ21件、東アジア12件であった。国別では、アメリカ合衆国に続き中国7件、カナダ6件であった。その他の国は各々1~4件の実施数であった。先に述べた通り、アメリカ合衆国ではFDAに医薬品を申請するために、その臨床試験をClinicalTrials.govへ事前登録することが義務化されているため、本件数の解釈には留意する必要があるが、ClinicalTrials.govによると、アメリカ合衆国が含まれる登録試験の割合は32%2)であり、この割合から見てもアメリカ合衆国におけるウェアラブルデバイスを活用した試験数は多いといえる。一方で、日本での試験数は前回の政策研ニュースで報告したアルツハイマー型認知症を対象疾患とした京都大学主体の試験1件のみであった。このことから、日本におけるウェアラブルデバイスの臨床試験活用は進んでいないことが明らかとなった。また、前回報告では10か国であったところ、今回の調査では21か国の登録が認められ、世界的には活用の裾野が広がっている様子がうかがわれた。
2-5 調査結果「対象疾患」
ウェアラブルデバイスを用いて実施された臨床試験の対象疾患を国際疾病分類第10版(以下、ICD-10疾病分類)(表1)で整理した結果を図5に示した。

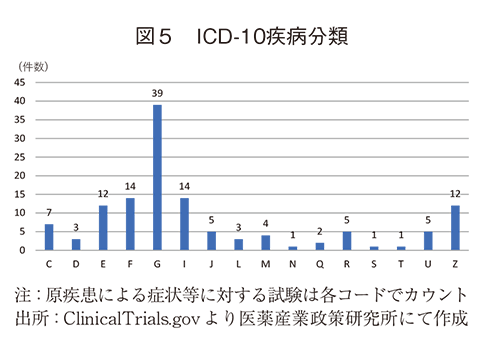
最も多くウェアラブルデバイスが活用されていた疾患領域はG:神経系の疾患39件であった。次いでF:精神および行動の障害14件、I:循環器系の疾患14件であった。個別の疾患では、前回報告と同様にパーキンソン病や心不全を対象とする試験が多く見られた他、各種がんやCOVID-19急性期後症候群、肥満などの疾患での活用が複数件認められ、ウェアラブルデバイスは更に広い範囲の疾患で活用が進んでいることが示された。
2-6 調査結果「測定項目」
ウェアラブルデバイスによる測定項目を図6に示した。
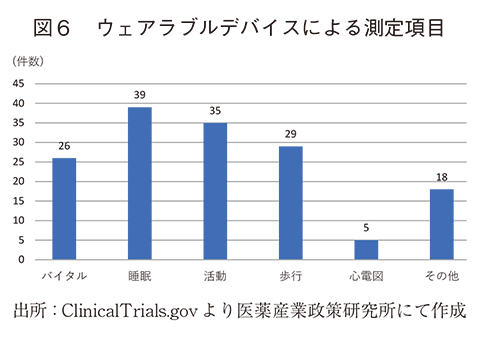
最も多かったのは、睡眠に関する測定39件であった。総睡眠時間、浅い/深い睡眠時間、覚醒回数など睡眠パターンや質を評価するものが中心であった。次に身体活動の測定が多く見られ35件で、活動時間、活動量が測定されていた。さらに、歩行測定が29件(歩数、歩行速度など)、バイタルが26件(心拍数、呼吸数、血中酸素飽和度など)と続いた。その他として、咳回数、まばたき活動、発作頻度や強さ、パーキンソン病の運動測定などが含まれていた。
3. ウェアラブルデバイスの活用用途
近年、ウェアラブルデバイスの測定範囲は拡大し、夜間の掻破動作や咳嗽頻度、運動緩慢・不随意運動・振戦などといった運動指標を含む多様な生体情報を、連続的かつリアルタイムで取得可能となった。
これにより、従来は客観的評価が困難であった臨床イベントの定量化や、複数の指標を統合的に解析することで病態の包括的評価が可能となり、ウェアラブルデバイスの活用は質的な進化を遂げている。
本節では、前節までの定量的分析から視点を転じ、前回の報告以降に顕在化したウェアラブルデバイスの代表的な活用事例について、関連文献を基に紹介する。
3-1.従来は客観的評価が困難であった臨床イベントの定量化
患者の主観的評価に大きく依存していた疾患特有のイベントを、客観的なデジタル指標として直接捉える技術が確立されたことは、近年の重要な進展の一つである。
音響モニタリングによる咳の客観的評価
慢性咳嗽治療薬GefapixantのPhase3試験で、英国のVitalograph社製の携帯型デジタル音響録音装置VitaloJAKTMが用いられた。患者が本デバイスを24時間携帯し、コンピューターアルゴリズムとアナリストにより、「24時間咳嗽頻度の平均変化量」を客観的に算出するものである。この「24時間咳嗽頻度の平均変化量」は、有効性を評価する主要評価項目として採用され、本薬はプラセボに対し有意に咳嗽頻度を減少させることが証明されている3、4)。
加速度センサーによる睡眠中掻爬行動の定量化
アトピー性皮膚炎治療薬BaricitinibのPhase3試験で、英国のActivinsights社製のウェアラブルセンサー「GENEActiv」が用いられた。本デバイスは、手首に装着する三軸加速度計であり、睡眠中の腕の動きを連続的にデータとして記録し、掻爬行動に特有のパターンを専用のアルゴリズムを用いて識別・定量化するものである。これにより、夜間掻痒の持続時間と強度、睡眠時間の割合、入眠後の覚醒時間などのデジタルエンドポイントが算出され、治療効果の評価に活用されている5)。
3-2.複数の指標を統合解析することによる病態の包括的な評価
単一のデバイスで、複数の異なる指標を同時に、かつ連続的に測定し、それらを統合解析することで、より複雑な病態を包括的に評価するアプローチも実用化されつつある。
多角的運動指標の統合によるパーキンソン病症状の評価
パーキンソン病治療薬のFoslevodopa/FoscarbidopaのPhase3試験で、米国のGlobal Kinetics社製のウェアラブルデバイス「Personal Kineti-Graph Ⓡ(以下、PKG)」が用いられた。PKGは、手首に腕時計のように装着する加速度計から得られるデータを、パーキンソン病に特化したアルゴリズムで解析し、運動緩慢(ブラジキネジア)、不随意運動(ジスキネジア)、振戦といった複数の運動指標を同時に定量化し、さらに薬剤効果のオン・オフ状態を連続的に可視化する。これにより、薬剤が日常生活下で運動症状全体をいかに安定的かつ包括的にコントロールするかを、客観的データとして実証できる。その上で、「PKGによって測定されたジスキネジア及びブラジキネジアのスコア(中央値及び四分位範囲)の変化」は、副次評価項目の一つとして、採用されている6、7)。
以上の事例が示すように、医薬品開発におけるウェアラブルデバイスの活用は、単に活動量を測るだけでなく、咳の回数のような具体的な症状や、複数の情報を組み合わせた疾患全体の評価へと、その役割を大きく広げており、医薬品の有効性を多角的かつ客観的に証明するための、極めて有用なツールへと進化を遂げつつある。
4. ウェアラブルデバイスを臨床試験で活用する際の課題
ウェアラブルデバイスを用いることで、試験参加者や患者の解釈、記憶、判断に依存しない(バイアスのない)、より客観的なデータを収集することができ、診察や検査では収集が難しかった日常生活の生体反応(運動、睡眠、発作等)に関するデータを、連続的かつタイムリーに収集し、可視化することができる。さらに、発作や服薬状況等を確認できるウェアラブルデバイスと医療機関が相互に通信することで、リアルタイムな試験参加者や患者へのサポートが可能となる。
しかし、医薬品開発でこのような多種多様なデータを活用する上では課題となる点も存在する。以下に主な課題を挙げる。
① データの正確性と解釈
ウェアラブルデバイスは通常、機器そのものの品質に加え測定環境やユーザーの装着方法、センサーの性能や装着位置などの影響を受けやすく、ノイズやばらつきを含む可能性がある。そのため、膨大かつ多様なデータをどのように解釈し、臨床的に有用な情報として活用するかに加え、信頼性のある基準値の設定も含めた新たな課題への対応が求められる。
② 評価指標とデバイス間の標準化の妥当性
ウェアラブルデバイスによって収集されるデータや評価指標が、患者にとって真に意味のある、価値あるアウトカムを適切に反映しているかどうかを検証することが求められる。一方、ウェアラブルデバイスの多様化により、デバイス間の標準化が不十分であり、異なる機器から得られたデータの比較や統合が困難となっている。このことは、アウトカムの解釈や結果の一般化に影響を及ぼす可能性がある。
③ プライバシーとデータセキュリティの懸念
ウェアラブルデバイスは個人の健康データを扱うため、プライバシーやデータのセキュリティに関する懸念が高まる。法律や規制に従った適切な管理に加え、データ漏洩や不正利用のリスクを低減させるため、十分な対策を講じる必要がある。
④ 参加者の遵守(アドヒアランス)
ウェアラブルデバイスの活用が求められる試験では、参加者がデバイスを適切に着用し続けることが重要となる。デバイスの着用を拒否したり、頻繁に外したりする参加者がいると、データの収集が不完全になる可能性がある。さらに、高齢者やデジタル機器に不慣れな参加者にとっては操作そのものがハードルとなる場合がある。
⑤ 規制・承認上の課題
ウェアラブルデバイスで得られたデータを薬事承認に用いる場合、評価基準や承認プロセスが明確化されていない領域が多く存在する。そのため、従来の評価項目とのバリデーションが必要であり、臨床試験における適切な位置づけを確立することが求められる。
5. まとめと考察
ウェアラブルデバイスは、臨床試験の多様な場面で活用が試みられ、新たな可能性を示している。これらのデバイスは、心拍数、歩数、血圧、睡眠状態などの生理的データをリアルタイムで収集できるため、医療研究におけるデータ収集の方法を根本的に変えつつある。リアルタイムでのデータ収集の能力は、従来の自己報告や定期的な診察に頼った評価方法を補完し、試験参加者の健康状態を客観的かつ連続的にモニタリングすることを可能とする。このようにして得られた詳細なデータは、治療効果の精緻な評価や副作用の早期発見、更には患者のライフスタイルの変化の把握といった臨床研究の質的向上に寄与する。
本稿におけるウェアラブルデバイスの臨床試験における活用の実態調査の結果、Phase2およびPhase4における活用促進が認められた一方で、Phase3での活用は、前回報告からの大きな増加は認められなかった。Phase3試験は医薬品の有効性と安全性を最終的に検証し、承認申請の根拠となるデータを取得することが主な目的となるため、活用するウェアラブルデバイスに求められる要件は厳しくなる。データの精度や信頼性、評価項目としての科学的妥当性が担保され、臨床試験の実施に関する基準であるGood Clinical Practiceに準拠したデータの完全性などといった要件が、ウェアラブルデバイスをPhase3試験で活用する大きな障壁となっている可能性が考えられた。
また、今回の分析では、日本の臨床試験におけるウェアラブルデバイスの活用事例は前回報告から増加していなかった。この点に関連し、日本製薬工業協会 医薬品評価委員会 データサイエンス部会が実施した調査では、活用にあたり以下のような課題が報告されている8)。
① 試験設計との適合性の問題
「ウェアラブルデバイスの活用に適した試験がない」
② 技術的/運用的な課題への対応力不足
「膨大なデータのハンドリング、分析とそのトレーニング」、「取得中データのモニタリング頻度や方法の検討」、「被験者側の負担(充電作業・同期の手間、長時間装着への抵抗感等)」、「評価指標が確立されていない」、「ウェアラブルデバイスのバリデーションの進め方」
③ ベンダー・デバイス選定に関する情報不足及び信頼性懸念
「適切な機器とベンダーの選定」、「デバイスの信頼性確保」、「グローバル試験でデバイスの各国承認状況が異なる場合の対応」
ウェアラブルデバイスの技術は日々進化しており、AIなど先進的な技術との統合により、新たな評価指標や解析手法が実現し、臨床評価の高度化を通じて医療への更なる貢献が期待される。しかし、日本が世界でのウェアラブルデバイスの活用動向に合わせ、これらを活用できる規制環境の整備や課題の克服ができなければ、こうした革新的技術を活用したグローバル臨床試験から取り残されるリスクが生じるであろう。
ウェアラブルデバイスは臨床試験におけるデータ収集の方法を革新する可能性を持っている。上記課題への対応を含めた今後のデジタル化の推進が急務といえる。
謝辞:本稿の作成に当たりご協力、ご助言をいただいた元医薬産業政策研究所 中塚靖彦主任研究員に心より感謝の意を表す。
注:本稿の一部内容は、『薬剤学』第86巻第1号(2026年1月)に掲載の論文「医薬品開発におけるウェアラブルデバイスの活用状況-2025年6月までの動向分析-」9)をもとに再構成したものである。
-
1)医薬産業政策研究所、「医薬品開発におけるウェアラブルデバイスの活用状況」、政策研ニュース No.63(2021年7月)
-
2)
-
3)McGarvey LP, et al.,“ Efficacy and safety of gefapixant, a P2X3 receptor antagonist, in refractory chronic cough and unexplained chronic cough (COUGH-1 and COUGH-2):results from two double-blind, randomised, parallel-group, placebo-controlled, phase 3 trials.” Lancet, 399(10328), 909-923, 2022.
-
4)Muccino, DR, et al.,“ Design and rationale of two phase 3 randomised controlled trials( COUGH-1 and COUGH-2) of gefapixant, a P2X3 receptor antagonist, in refractory or unexplained chronic cough.” ERJ Open Research, 6(4), 2020
-
5)Ji J, et al., “Assessing treatment effect of baricitinib in atopic dermatitis using digital endpoints derived from actigraphy data:nocturnal scratch and sleep disturbance. J Invest Dermatol.” 143(11 Suppl):S364. Abstract 192, 2023.
-
6)Soileau M J, et al., “Safety and efficacy of continuous subcutaneous foslevodopa–foscarbidopa in patients with advanced Parkinson ’s disease:a randomised, double-blind, active-controlled, phase 3 trial.” Lancet Neurol, 21(12):1099-1109, 2022
-
7)U.S. Food and Drug Administration. Clinical Review:NDA 215804 Foslevodopa-Foscarbidopa (Vyalev)[Internet]. Silver Spring( MD):FDA;2022
-
8)日本製薬工業協会 医薬品評価委員会 データサイエンス部会 2023年タスクフォース1-2「DCT の導入状況およびDCT の各手法に関するアンケート結果」、2024年10月
-
9)日本製薬工業協会 医薬産業政策研究所「医薬品開発におけるウェアラブルデバイスの活用状況-2025年6月までの動向分析-」、薬剤学、86(1)、2026年1月

