目で見る製薬産業 アンメット・メディカル・ニーズに対する医薬品の開発状況 -2020年の動向-
医薬産業政策研究所 主任研究員 中尾 朗
はじめに
医薬産業政策研究所では、公益財団法人ヒューマンサイエンス振興財団(以下、HS財団)による医療ニーズに関する調査結果1)をもとに、新薬の承認及び開発パイプラインに関するデータを集計し、アンメット・メディカル・ニーズに対する製薬企業の取組み状況を継続的に分析している2)、3。
前回の政策研ニュースNo.59(2020年3月)では2014年度の治療満足度調査の結果に基づき、60疾患に対する2020年1月時点での開発パイプライン数及び2011年~2019年の薬剤承認数を示すとともに、60疾患に含まれる10のがん種に対する薬剤の承認件数の増加数と5年生存率の改善度との関係を分析した。本稿では2020年3月に発行された「60疾患に関する医療ニーズ調査(第6回)」を元に、最新60疾患に対する2020年8月末時点での開発パイプライン数を示すとともに、新たに60疾患に加わった8つの疾患(但し2つの新疾患は従来カバーしてきた疾患の分割)の中からいくつか選択した疾患について、既承認医薬品、開発品について調査した結果を報告する。
治療満足度別にみた新薬の開発状況
図1は2019年度HS財団調査における治療満足度4)(横軸)、薬剤貢献度5)(縦軸)に沿って疾患をプロットし、今回調査した開発品目数6)を円の大きさおよび数値で示したものである。前回調査と同様の製薬会社20社7)の2020年8月末日時点における国内開発品目(フェーズ1~申請中)を集計対象とした8)。該当の開発品目数は284件9)であり、そのうち新規有効成分(NME)の数は122件(43%)であった。前回調査同様に、60疾患開発品目数におけるがん疾患の開発品目数割合が非常に高く、その割合は50%(143/284)であった。がん10種開発品目数におけるNME数は44件であり、割合にすると31%(44/143)であった。がん疾患におけるNME率が全体と比較して低いことは1つの薬剤を複数のがん疾患で、あるいは同一がん疾患をより細分化して開発することが多いことによるものと考えられる。
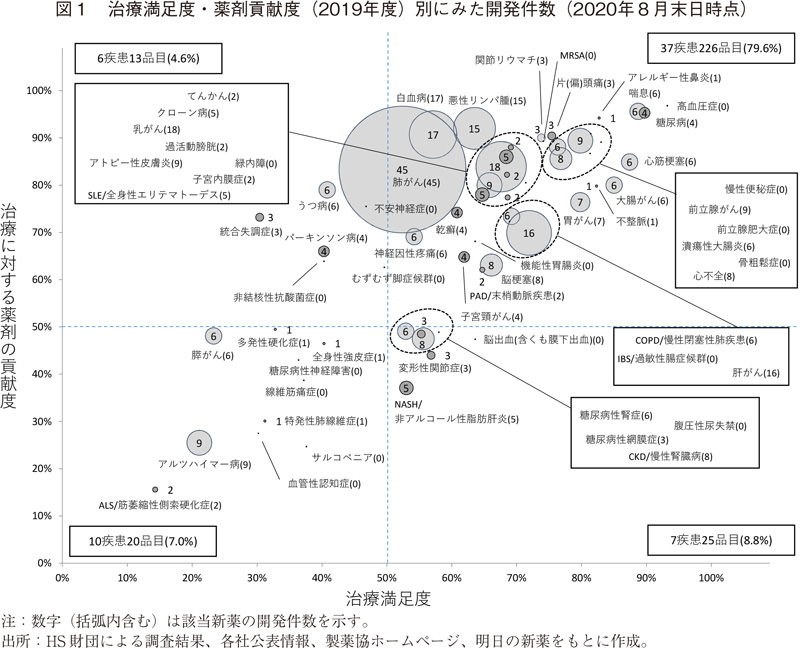
今回調査と前回調査の大きな相違点としては、治療満足度が50%以上かつ治療に対する薬剤貢献度50%を示す領域、いわゆる第一象限の開発品目数割合が64.4%から79.6%へと増加したことであった。これは60疾患の中で最も開発品目数が多い「肺がん」の治療満足度が2014年度調査から2019年度調査にかけて37.3%から52.4%へ向上した9)ことによるものであると考察された。これに連動して治療満足度が50%以下かつ治療に対する薬剤貢献度50%以上を示す領域(第二象限)の開発品目数割合が29.2%から4.6%へと減少した。
60疾患のうち第一象限に含まれる疾患の比率が61.7%(37/60)であることと比較し、本領域に含まれる開発品目数(79.6%)はかなり多い。ただ、60疾患中の10疾患ががん疾患であり、膵がん以外の9がん疾患が第一象限に含まれていること、さらに例えば血液がんの一種である「白血病」は大きく分けても「急性・慢性」×「リンパ性・骨髄性」=4種に分類されるように一口に「〇〇がん」と言っても種類は多種多様であること、などから9がん疾患が含まれる第一象限の新薬開発品目比率が高いのは道理に適ったものと思われた。
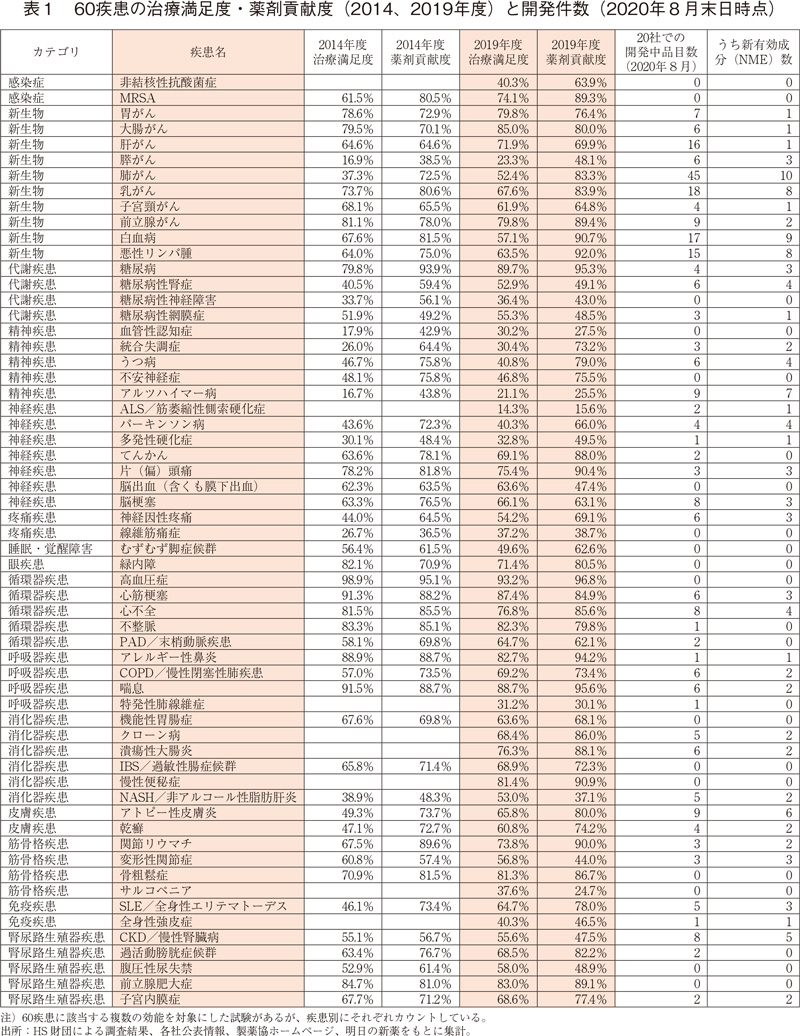
治療満足度、薬剤貢献度を示すパーセントが共に50を超えているとしても、その満足度、貢献度の内訳は「ある程度満足(貢献)」が「十分に満足(貢献)」を大きく上回っている。また100に至っていない残りのパーセントの多くは「不満足」「あまり貢献していない」であるが、中には「治療が行えているとはいえない」「効く薬がない」との回答も含まれている。このようなことから、たとえ第一象限にある疾患であろうとも、まだまだ医薬品が疾患治療へ貢献できる余地は十分にあり、かつそれが求められていると考えられた。参考として、2014年度と2019年度のHS財団調査結果、および2020年8月末日時点における製薬20社の疾患ごとの開発品目数、およびNME数をまとめたものを表1に示す。
新たに加わった8疾患
今回のHS財団による医療ニーズ調査では、医療環境の大きな変化を鑑みて、一部疾患の入れ替えが行われた。調査班による報告書の文言を借用すると、除外された8疾患は医療満足度・薬剤貢献度が高い疾患として「高尿酸血症・痛風」「脂質異常症」「慢性C型肝炎」「慢性B型肝炎」「HIV/エイズ」および「副鼻腔炎」の6疾患、治療が医薬品主体ではない「睡眠時無呼吸症候群」、そして「潰瘍性大腸炎」と「クローン病」の総称である「IBD/炎症性腸疾患」の合計8疾患が除外され、新たな疾患として、新たな診断・治療法、医薬品等の開発が望まれる疾患として多く挙げられた「ALS/筋萎縮性側索硬化症」「非結核性抗酸菌症」「特発性肺繊維症」「全身性強皮症」そして「IBD/炎症性腸疾患」を「潰瘍性大腸炎」と「クローン病」に分けた6疾患に加え、困っている人が多く近年新薬が上市された「慢性便秘症」、そして高齢者の増加で大きな問題となっている「サルコペニア」の2疾患の合計8疾患が追加された。
新たに加わった8疾患の薬剤承認件数
今回新たに加わった8疾患のうち、「潰瘍性大腸炎」と「クローン病」は、これまで「IBD/炎症性腸疾患」として承認品目数および開発品目数の調査を行っていたが、残りの6疾患についてはこれまで調査したことがなかった。そこで、今回は2007年から2019年までの過去13年間の上記8疾患の新薬承認状況を新有効成分含有医薬品および新効能医薬品を対象に調査した11)。
表2に示す通り、承認品目数の多い順に「潰瘍性大腸炎」(新有効成分1、新効能5)、「慢性便秘症」(新有効成分3、新効能2)、「非結核性抗酸菌症」(新有効成分1、新効能4)、「クローン病」(新効能4)、「特発性肺線維症」(新有効成分2)、「全身性強皮症」(新効能2)、「ALS/筋萎縮性側索硬化症」(新効能1)であった。「サルコペニア」は2007年以前も含め承認された医薬品が1剤も無いという結果であった。

承認品目数が4つ以上の「慢性便秘症」「クローン病」「潰瘍性大腸炎」の2019年度の医療ニーズ調査結果における治療満足度、薬剤貢献度はともに60%を超えており、新規医薬品が疾患治療にもたらす効果が伺えるが、過去13年間に5品目の新薬が承認された「非結核性抗酸菌症」の治療満足度は40.3%(薬剤貢献度は63.9%)と低い値であった。承認品目が2つ以下であった「特発性肺線維症」、「全身性強皮症」、「ALS/筋萎縮性側索硬化症」、「サルコペニア」においては、治療満足度、薬剤貢献度ともに50%を切っており、中でも「ALS/筋萎縮性側索硬化症」は、治療満足度、薬剤貢献度ともに60疾患の中でもっとも低い値(治療満足度14.3%、薬剤貢献度15.6%)であった。
新たに加わった8疾患の医薬品開発件数
表1に示した通り、製薬20社の2020年8月末日時点における新8疾患の開発品目数はそれぞれ、「ALS/筋萎縮性側索硬化症」2品目、「非結核性抗酸菌症」0品目、「特発性肺繊維症」1品目、「全身性強皮症」1品目、「潰瘍性大腸炎」6品目、「クローン病」5品目、「慢性便秘症」0品目、「サルコペニア」0品目であった。「慢性便秘症」は過去13年間で5つの新薬が承認され、2019年度調査において治療満足度が81.4%、薬剤貢献度が90.9%であったこと、「クローン病」「潰瘍性大腸炎」においては比較的開発品目数が多いことから、今後のさらなる治療満足度と薬剤貢献度の向上が予想された。しかし残りの5疾患については、医療満足度・薬剤貢献度がそれほど高くないにも関わらず開発件数が非常に少ないことが分かった。
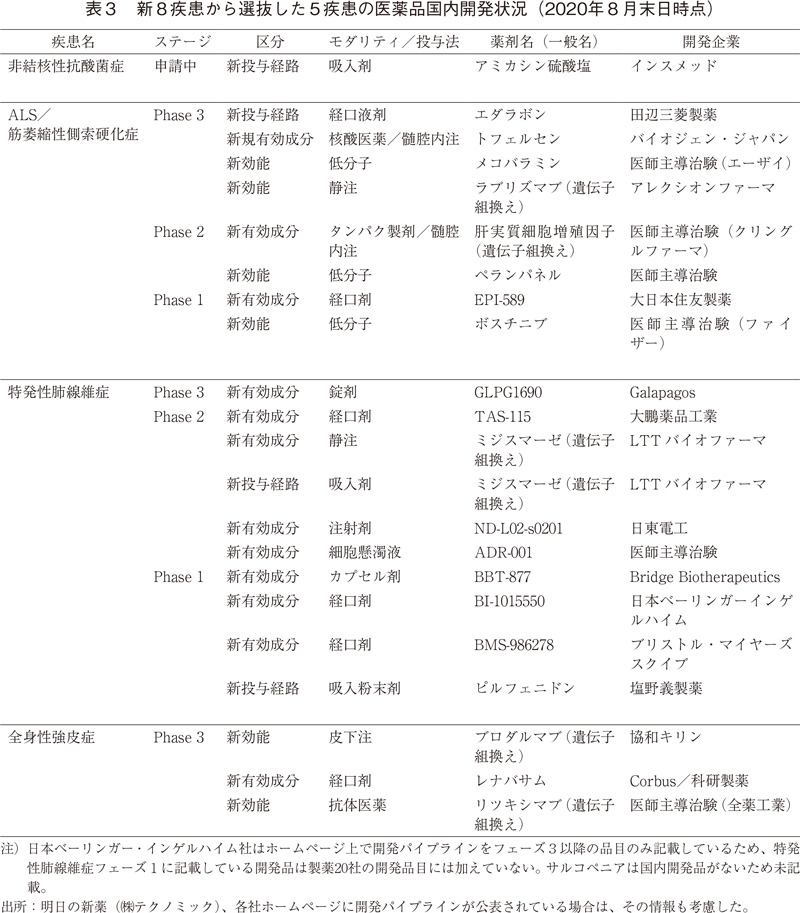
これら低い開発件数が日本国内での医薬品開発の現状なのか、たまたま調査対象の製薬20社の開発件数が少なかっただけなのかを調査することにした。具体的には調査対象を製薬20社に限定せず、国内開発品目検索を「明日の新薬((株)テクノミック)」の国内検索機能を用いて実施し、開発対象をフェーズⅠから申請中までとした。なお、「サルコペニア」は明日の新薬では「筋肉減少症」として検索した。企業のホームページに開発パイプラインが記載されている場合はその情報も考慮した。その結果、「特発性肺線維症」は10品目(うちNME8品目、企業開発品9品目)、「ALS/筋萎縮性側索硬化症」8品目(うちNME3品目、企業開発品4品目)、「全身性強皮症」3品目(うちNME1品目、企業開発品2品目)、「非結核性抗酸菌症」1品目の開発が行われていることが分かった。これら開発品の中から新薬が承認、上市され、治療満足度・薬剤貢献度が向上することが期待される。
一方、「サルコペニア」においては、調査対象を広げても開発品目がないことが分かった。一般社団法人日本サルコペニア・フレイル学会によると、2017年末にサルコペニア診療ガイドラインが初めて作成されたが、現段階でエビデンスレベルの高い治療・予防方法はないとのことである12)。今後、疾患の発症メカニズムが明らかにされ、エビデンスレベルの高い疾患の予防、治療法が見いだされることに期待したい。
-
1)公益財団法人 ヒューマンサイエンス振興財団「2019年度 国内基盤技術調査報告書-60疾患に関する医療ニーズ調査(第6回)-」
-
2)医薬産業政策研究所「アンメット・メディカル・ニーズに対する医薬品の開発・承認状況」政策研ニュースNo.34(2011年11月)、No.38(2013年3月)、No.52(2017年11月)、No.59(2020年3月)
-
3)医薬産業政策研究所「アンメット・メディカル・ニーズに対する医薬品の開発状況」政策研ニュースNo.41(2014年3月)、No.45(2015年7月)
-
4)HS財団の医療ニーズ調査では、アンケート回答の4つの選択肢(十分に満足/ある程度満足/不満足/治療が行えているとはいえない)のうちの「十分に満足」と「ある程度満足」を合計した割合(%)を医療満足度としている。
-
5)HS財団の医療ニーズ調査では、アンケート回答の4つの選択肢(十分に貢献/ある程度貢献/あまり貢献していない/効く薬がない)のうちの「十分に貢献」と「ある程度貢献」を合計した割合(%)を治療に対する薬剤の貢献度としている。
-
6)公益財団法人 ヒューマンサイエンス振興財団「2019年度 国内基盤技術調査報告書-60疾患に関する医療ニーズ調査(第6回)-」
-
7)対象企業はアステラス製薬、アストラゼネカ、エーザイ、大塚製薬、小野薬品工業、グラクソ・スミスクライン、協和キリン、サノフィ、塩野義製薬、第一三共、大日本住友製薬、武田薬品工業、田辺三菱製薬、中外製薬、日本イーライリリー、日本ベーリンガー・インゲルハイム、ノバルティスファーマ、バイエル薬品、ファイザー、MSDである。
-
8)データソースは各社ホームページ・決算資料、日本製薬工業協会ホームページ、「明日の新薬」((株)テクノミック)を用いた。ただし、上記3つのデータソースで「明日の新薬」のみに記載されている開発パイプラインは加えていない。
-
9)60疾患に該当する複数の効能を対象にした試験があるが、疾患別にそれぞれカウントした。
-
10)2014年度調査の治療満足度37.3%は「十分満足(3.6%)」と「ある程度満足(33.7%)」の合計、2019年度調査の治療満足度52.4%は「十分満足(8.7%)」と「ある程度満足(43.7%)」の合計である。
-
11)厚生労働省薬事・食品衛生審議会部会審議品目又は報告品目における新有効成分含有医薬品(NME)・新効能医薬品を集計対象とした。
-
12)

