Opinion Beyond-The-Pillに関する我が国の現状の制度概要
医薬産業政策研究所 主任研究員 枡田竜育
はじめに
Beyond-The-pillあるいはAround-The-Pillとのキーワードは、定義が明確でないだろうが、数年前から業界内外で叫ばれている。国内製薬企業が医療用医薬品製造販売業に特化するのか、あるいは一般用医薬品製造販売業はもとより医療機器製造販売業その他多角的な事業展開を行うのか、いずれも個社の経営判断であり、本稿の目的はその是非を論じることにはない。一方、Beyond-The-Pillなどについて、医薬品産業に従事する立場で一顧だにしないという状況ではなかろう。本稿は、製薬企業の視点から、ヘルスケアの分野において医薬品以外の事業を概観する際の基礎を示す。隣の芝が青いかどうかは別として、我が産業に従事する我々の将来の一燈となれば幸いである。
1.背景
医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下、薬機法)は、疾病の診断、治療又は予防に使用される医薬品や医療機器などを対象として薬事行政の基礎をなし、我が国の保健衛生の向上に貢献している。一方、医療を、介護、健康増進あるいは予防、そして健康に関係する商品やサービスとあわせてより広くヘルスケアサービスとして捉える1)と、ヘルスケアサービスには現時点でも膨大な選択肢が存在する。この膨大な商品・サービスの大洋を製薬企業から見ると、Beyond-The-PillあるいはAround-The-Pillということになるのだろう。とりわけデジタル分野での技術進展をはじめ、患者あるいは健常者に対してヘルスケアに関する効用をもたらす新たな商品・サービスのへの期待が高まっている。デジタルセラピューティクス(DTx)は、米国では既に業界団体"Digital Therapeutics Alliance"が設立され活動している2)が、我が国でもニコチン依存症治療用アプリが医療機器として承認申請され3)、DTxについて認知が進んできたのではないだろうか。製薬企業においても、Around-The-PillあるいはBeyond-The-Pillなどと報じられる4)、医薬品に付随するサービスあるいは医薬品以外の事業へのビジネスとしての参入や検討が進められている。
我が国では、健康・医療戦略において「次世代ヘルスケア産業」の振興が経済産業省などにより図られている。
経済産業省は、図1のようにヘルスケアの分野における公的保険外サービスの産業群を示し、2025年には市場規模が約33兆円に及ぶとの見通しを示している。この図は「卵の図」と呼ばれることもあるようだが、端的に理解するとすれば、黄色地(卵の黄身)は我が国の厚生行政の責任を担ってきた厚生労働省の管轄分野で、白地(卵の白身)は経済産業省等が構想する分野ということになろう。
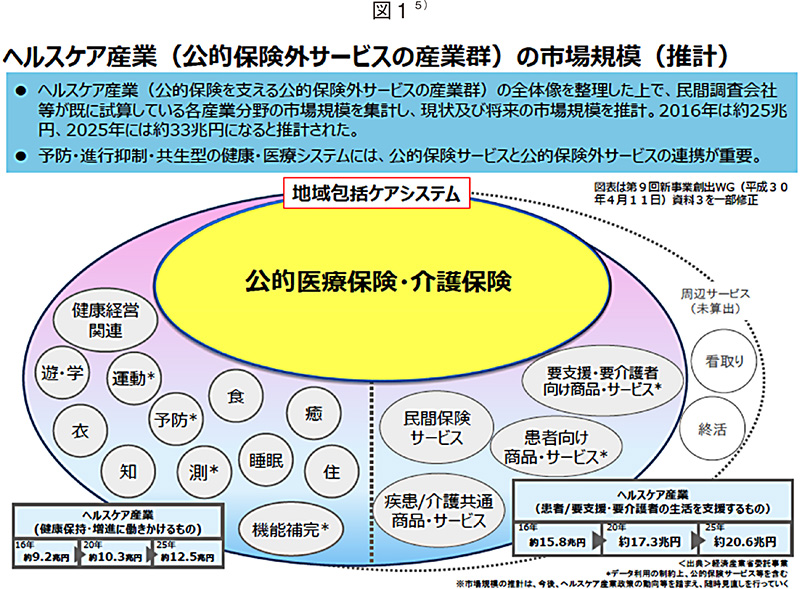
この白地部分のサービスにおいては、これから生み出されるものも含め、ヘルスケアに大いに資する商品・サービスも生まれてくるだろうし、一方で、玉石混淆となって消費者の不利益になることのないような仕組みを整備することも求められる。本稿は、白地部分について大きく「経口摂取するモノ」=医薬品と健康食品と、それ以外=医療機器とヘルスケア機器に分類し、それぞれについての規制の概要を俯瞰する。
2.医薬品と健康食品
医薬品の規制区分の概要については、本稿の主な読者には釈迦に説法であり触れることはしないが、薬機法において業許可と製造販売承認等による製造販売規制が設けられている。
(1) 健康食品の制度概要
医薬品等と食品は、我が国では明確に峻別されている7)。医薬品は、人の疾病の診断、治療又は予防に使用されることが目的とされているものであり、食品は医薬品及び医薬部外品以外のすべての飲食物である。また、食品には生命維持のための栄養面での働き(栄養機能・一次機能)や食事を楽しもうという味覚・感覚面での働き(感覚機能・二次機能)のほか、生体の生理機能を調整する働き(体調調節機能・三次機能)がある8)。この体調調節機能について、我が国では「健康や栄養に関する食品表示制度」として整備が進められてきた。2015年より施行された食品表示法により、食品の表示に関する包括的かつ一元的な制度が整備されている。「健康食品」は法律で定義されているわけではないが、図2の通り「保健機能食品」と「いわゆる健康食品」に大別される。
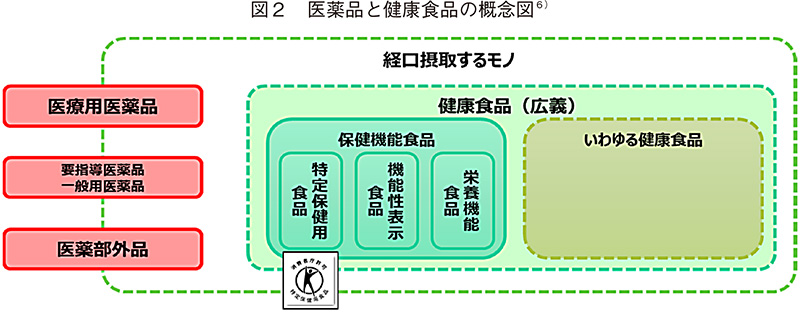

食品表示法で新たに機能性表示食品の制度が創設されたことから、2019年現在、保健機能食品は、特定保健用食品、機能性表示食品、栄養機能食品に分類される。
健康や栄養に関する現在の食品表示制度は、食品表示法制定前の課題、すなわち栄養機能食品については、対象成分が限定されていること、また特定保健用食品については、食品ごとに安全性や有効性に係る臨床試験が必須であるとともに許可手続に時間と費用がかかるため、中小企業にとってハードルが高いこと等を克服すべく、規制改革の取り組みを経て構築されている。また、健康食品の安全性を確保するための具体的な仕組みとしては、原材料の安全性の確保のための具体的方策、製造工程管理(GMP)、健康食品の安全性確保に係る第三者認証が挙げられる。
3.医療機器とヘルスケア機器
健康分野の機器・器具、あるいはアプリなども含めたデジタルツールは、現時点でも多種多様である。
薬機法で定める「医療機器」に限っても、診断系機器(内視鏡、CT、MRI等)、治療系機器(カテーテル、ペースメーカー等、その他があり、一般的な名称として4,000種類以上、品目数は30万以上とも言われている10)。医療機器以外にも、ヘルスケア機器(非医療機器)も膨大な商品・サービスが存在している。
(1) 医療機器
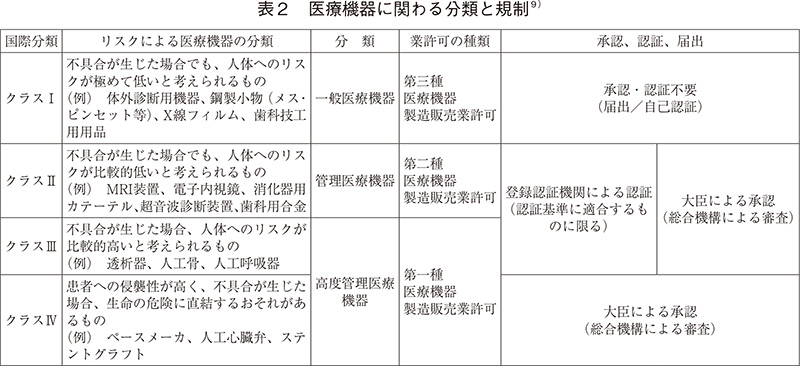
「医療機器」は、医薬品と同様に薬機法において業許可と承認等による製造販売規制が設けられている(図3)。「医療機器」は、リスクの程度によって分類が行われており、表2の通りである。医薬品と異なるのは、指定高度管理医療機器等について、薬機法に基づき、登録認証機関が認証を行う制度が設けられている点である11)。また、薬事法から薬機法への改正時に、新たにプログラム(ソフトウェア)を医療機器として製造販売の承認等の対象とすることとなった。医療機器プログラムの取り扱いにおいては、医療に関するプログラム全てを医療機器として取り扱うわけではなく、診断・治療等を目的としたプログラム単体が対象であり、通知で示されている12)。
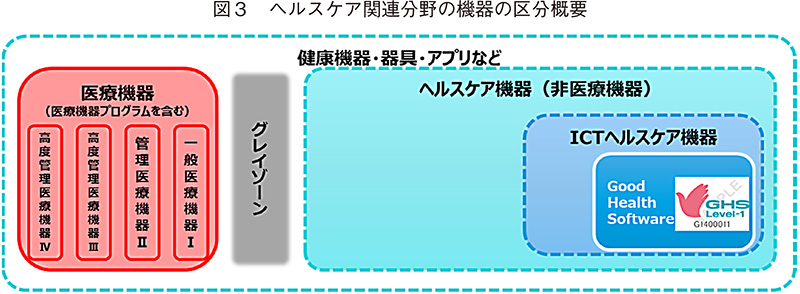
(2) ヘルスケア機器(非医療機器)
医療機器以外、すなわち薬機法の規制対象外はヘルスケア機器(非医療機器)と位置付けられている。ただし、グレイゾーンが存在すると位置付ける向きもあるし13)、「ヘルスケア機器」として販売されている製品やソフトウェアの中には、類似製品が「医療機器」の区分で発売されているなど、医療機器との区分があいまいな製品も存在する14)。
さらに、ICTを活用したヘルスケア機器については、2012年より経済産業省が産業振興と最適な制度設計の方向性を検討してきた。この検討を経て、2014年に産業界に一般社団法人ヘルスソフトウェア推進協議会(以下、GHS)が設立され、ヘルスソフトウェア開発ガイドラインを策定している。業界自主ガイドラインを設け、使用者が優良なヘルスソフトウェアを使用できる環境を整えた上で、利用者に分かりやすく伝えるべく、GHSは適合宣言マーク(GHSマーク)を定めている15)。
(3) ヘルスケアサービス
政府はヘルスケアサービスの品質評価の仕組みについて、業種ごと、あるいは業界横断での自主的な認証制度・ガイドライン策定等を促している。具体的には、経済産業省が2019年4月に策定した「ヘルスケアサービスガイドライン等のあり方(以下、「本指針」)」16)のなかで、業界団体等が策定するガイドラインや認証制度のあり方を提示している。本指針では、「ヘルスケアサービス」は、「健康の保持及び増進、介護予防を通じた健康寿命の延伸に資する商品の生産若しくは販売又は役務をいう。(ただし、個別法による許認可等が必要な商品や役務等を除く。)」と定義されている。本指針は、業界自主ガイドラインは、透明性、客観性、継続性の観点を踏まえて策定されるべきとしたうえで、これらの観点以外にも、ガイドラインの趣旨や目的、ヘルスケアサービスの要件の具体化や詳細化、安全性と効果に関する検証方法を含めた規約、広告表示のあり方などを位置付けることが必要であるとしている。

4.まとめ
「ヒト」は、本当に必要とするときに、適切な医療を受けられなければならない。「ヒト」がその恩恵に浴することができるよう社会は環境や制度を整えなければならない。しかし、「ヒト」にとって、最も望ましいのは生涯のなかで医療を受ける必要が生じないことである。必要な人に適切な医療を受けられるような環境を整備する以上の資源と努力を、医療を受ける必要をなくすことに注ぐべきかもしれない。医療を受けずに済むために、かかってしまった疾患と闘う力を強化するために、さらには、ヒトが、でき得る限り、長く活動と選択の自由をもっていられるために健康をつくるための医療を推進すべきである。
以上は、「日本の医療のグランドデザイン2030」(日本医師会総合政策研究機構)において、「あるべき医療」の一節に記されている文章である。
医療そして医療の重要なツールとして医薬品の価値が全く失われてしまうことはないだろうが、ここにもある通り、発症した疾病の治療のみならず罹患しないための介入や先制医療(発症前の介入)の実現が期待されている。この一翼を担うものとして、特にデジタル分野の著しい技術進歩を健康に関わる全く新しい商品やサービスに応用していくことが期待されている。DTxも含め、新たな商品・サービスについては、本稿で概観してきた規制区分の整備をはじめ、社会への実装に向けた仕組みが整備されつつある。このような新しい仕組みを国民に浸透させていくことは容易ではない。例えば本稿で俯瞰した食品表示制度にしても、行政、業界、各企業が様々な方法で周知を図っているが、各区分の意味を正確に理解している割合は、トクホで約35%、その他では10%台にとどまったとの調査もなされている17)。医薬品産業は「医薬品」についての啓発に勤しんできた経験を有する。健康に関わることといえども商品や産業についての国民的な理解を得ていくためには、継続した取り組みが必要となることは言うまでもない。まして、全く新しい商品・サービスとなると、開発に掛かる労力もさることながら、国民が安心して選択できる環境を新たに整備していくことも重要となる。その中では、有効性や安全性を証明する膨大な経験値と世界の患者さんの治療に貢献してきた豊富な実績を有する製薬企業あるいはその業界団体が、ヘルスケアサービスにおけるルールづくりに積極的な役割を果たす意義は、決して少なくない。例えば、Evidence Basedの考え方やその証明プロセス、安全性の確保と有事の対応、供給責任、医療分野との緊密な連携に基づく事業運営など、医薬品産業が培ってきた膨大な経験のノウハウが活きると考えられる。
ヘルスケアの新たな商品・サービスが生み出される先に、我々の産業のコア・コンピタンスがある日突然大幅に陳腐化しかねないというのは、愚にもつかない杞憂にすぎないだろうか。創薬を通じ、医薬品が引き続き治療や健康増進の本質を担うモノとして、産業が人類に貢献し続ける存在であり続けることを期待したい。その中では、医薬品以外の商品・サービスがヘルスケアの分野にもたらす効用、およびその政策制度の動向にも注視が必要となろう。ヘルスケアサービスという広大な大洋の中で、患者さんや生活者に思いを馳せるとき、クスリに軸足を置いてBeyond-The-Pillで着想する医薬品産業であるからこそ果たせる貢献があるものと考える。
以上
-
1)医療がサービス業であるか否かについては、医療の本質に関わる繊細な議論があるが、本稿の趣旨からは強く拘ることなく、広い概念としての「ヘルスケアサービス」には医療を含むものと位置付ける。
-
2)
-
3)
-
4)Beyond-The-PillあるいはAround-The-Pillの明確な定義はないが、筆者としては以下のように定義を試みる。すなわち、Around-The-Pillとは製薬企業が新たな業許可を取得することなく提供可能な事業を指す。Beyond-The-Pillとは製薬企業が新たな業許可を取得することではじめて提供可能となる事業を指す。いかがであろうか。
-
5)健康・医療戦略推進本部に設置されている「次世代ヘルスケア産業協議会」において、2019年4月12日に事務局が示した「次世代ヘルスケア産業協議会の今後の議論について」の中で、本図が取り上げられている。
-
6)「いわゆる健康食品について」、東京都福祉保健局健康安全部薬務課より著者作図
-
7)食品衛生法では、「この法律で食品とは、全ての飲食物をいう。ただし、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和三十五年法律第百四十五号)に規定する医薬品、医薬部外品及び再生医療等製品は、これを含まない。」と定められている。また、食品表示法では、「「食品」とは、全ての飲食物(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和三十五年法律第百四十五号)第二条第一項に規定する医薬品、同条第二項に規定する医薬部外品及び同条第九項に規定する再生医療等製品を除き、食品衛生法第四条第二項に規定する添加物(第四条第一項第一号及び第十一条において単に「添加物」という。)を含む。)をいう。」とされている。
-
8)「食品の新たな機能性表示制度に関する検討会報告書」2014年7月
-
9)
-
10)
-
11)
-
12)
-
13)医療機器のソフトウェアの考え方は「薬食監麻発1114 第5号 平成26年11月14日」内に詳細に記されている。この中には「医療機器に該当しないプログラム」としての除外事項の記載がある。除外事項の一つとして、「一般医療機器(機能の障害等が生じた場合でも人の生命及び健康に影響を与えるおそれがほとんどないもの)に相当するプログラム」が掲げられており、一般医療機器は医療機器であるにもかかわらず、一般医療機器に相当するプログラムは、一般医療機器ではないということとなる。この矛盾した要素が、ソフトウェアにおける医療機器クラス分類上のグレイゾーンである。
-
14)
-
15)
-
16)「ヘルスケアサービスガイドライン等のあり方」、経済産業省、2019年4月
-
17)「食品表示に関する消費者意向調査」、消費者庁

