くすりの情報Q&A Q40.「ジェネリック医薬品」とは、なんですか。
回答
先発医薬品の再審査が終了し、その製品の特許が切れた後に、その他の製薬企業が後発で製造・販売する医薬品です。「先発医薬品と同じ有効成分を、同じ量含んでおり、同等の効能や効果が得られる」と認められた医薬品です。後発医薬品とも呼ばれます。
解説
ジェネリック医薬品は、先発医薬品のように何百億円ともいわれる多額の研究・開発費を使わずに製造・販売されますので、その分、薬価は安く設定されます。先発医薬品の3~6割程度の薬価です。
日本の医療保険制度は、昭和36(1961) 年に「国民皆かい保険」を達成して以来、一定の自己負担で必要な医療サービスが受けられる体制を整備することにより、世界最長の平均寿命や高い保険医療水準を達成してきました。しかし、医療技術の進歩や高齢化などにより、今後とも医療費の上昇が見込まれ、皆保険を維持していくためには、必要な医療を確保した上で、可能なものは効率化を図ることが重要となってきました。ジェネリック医薬品の使用促進により、医療の質を落とすことなく、薬剤費の負担を軽減しつつ、より革新的な新薬を医療保険で高く評価することによって、その開発を促うながすなど、限られた医療の財源をより有効に活用することも可能となるのです。そこで厚生労働省は、平成25年4月に、ジェネリック医薬品の『安定供給』『品質に関する信頼性の確保』『情報提供の方策』『使用促進に係る環境整備』などの内容を盛り込んだ「後発医薬品のさらなる使用促進のためのロードマップ」を策定し、平成30年3月末までにジェネリック医薬品の数量シェア60%以上を目標に掲げ、都道府県や製薬企業、保険者などと協力して普及促進に取り組んでいます。私たちの身近なところでは、処方箋せんの記載内容が変更され、医師の指示がない限り、ジェネリック医薬品への変更が可能になっています。また、患者さん自身でも医師や薬剤師に対してジェネリック医薬品への変更を相談することも可能です。
図表・コラム
40|先発医薬品(新薬)とジェネリック医薬品
新薬の再審査期間と特許権存続期間の両方が満了すると、新薬と同じ有効成分の医薬品を、「ジェネリック医薬品(後発医薬品)」として他の製薬企業が製造・販売することが可能になります。ジェネリック医薬品を製造・販売する際には、厚生労働省により製造販売承認を取得することが必要です。このとき、先発医薬品と同等の品質、生物学的同等性が確保されていることを科学的に証明した資料などが求められます。
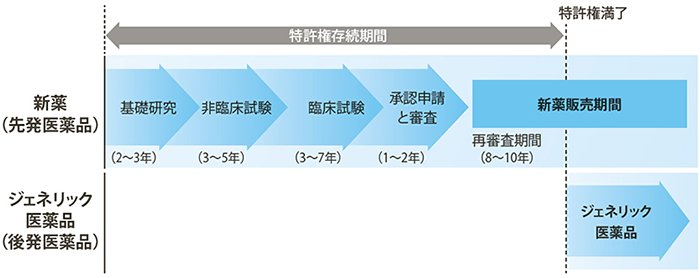 出典:「 製薬協ガイド」(2012-2013)より引用。
出典:「 製薬協ガイド」(2012-2013)より引用。




