医薬品評価委員会 企業事例から見えたJ-RMPのメンテナンス -適切な医薬品リスク管理のための提案-(令和4年3月版)
ファーマコビジランス部会
2022年3月
2014年10月に法制化された医薬品リスク管理計画書(J-RMP)は、現在多くの企業の医薬品にて作成され、リスク管理に役立てられています。
2020年、KT1は「RMPの評価」「J-RMP改訂後の周知方法」について、理想とする運用を「企業事例から見えたJ-RMPのメンテナンス(令和2年2月版)」にて提案しました。
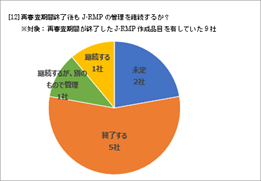
その後2年が経過し、再審査期間満了を迎えたJ-RMP策定品目も登場しはじめ、再審査申請資料作成を通して、安全性検討事項の評価を行い、J-RMPを終了する事例が集積されてきました。一方、J-RMP終了時の手順やRMP資材の取り扱い、シグナル評価手順等については、明確な指針等がなく各社で方法を模索している状況です。そこで、2021年度のKT-1参加16社に対して再度アンケート調査を実施し、再審査申請時及び再審査終了後の各社のJ-RMPの管理の実態、J-RMP終了のメンテナンスについて追記した令和4年3月版を作成しました。
なお、再審査申請にあたっては、追加のリスク最小化活動を評価することも必要となります。その留意事項については、KT-1が2021年6月に作成した「医薬品リスク管理計画(RMP) 追加のリスク最小化活動(資材)の効果を評価するための留意事項」もご参照ください。
本書を活用して頂き、J-RMPの運用に携わっている方々の日々の問題や疑問が解決できる一助になれば幸いです。
今回の成果物
留意事項
- 事例については限られた情報であり、また、実例そのものではなく事例としてわかりやすいように一部改変したものである点にご留意ください。
- 本書にて提案しました様式については、別途Wordファイルを掲載していますので、適宜ご活用ください。
医薬品評価委員会PV部会 継続課題対応チーム1(KT1)

